
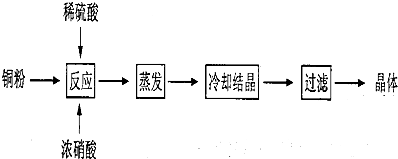
分析 (1)根据铜与浓硝酸反应的产物判断现象;
(2)根据反应物判断可能存在的杂质,溶解度不同的可溶性盐可用重结晶法分离;
(3)根据氢氧化钠的物质的量求出硫酸铜的物质的量,进而求出质量;
(4)测量固体的含量,要先称量一定质量的固体,经溶解、沉淀、过滤、干燥、称量等操作,要验证是否洗涤完全,向上层清液中继续滴加加氯化钡溶液,若有沉淀产生说明还没有沉淀完全.
解答 解:(1)铜与浓硝酸反应为:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,生成硫酸铜和二氧化氮气体,故答案为:溶液呈蓝色,有红棕色气体生成;
(2)混有硝酸铜杂质,需利用溶解度的不同,用重结晶的方法进行分离,故答案为:重结晶;
(3)根据化学方程式计算,所含硫酸铜晶体的质量为$\frac{0.1000mol/L×(28.00×1{0}^{-3}L-20.16×10{\;}^{-3}L)}{2}$×250g/mol═0.0980g,故答案为:0.0980g;
(4)测量固体的含量,要先称量一定质量的固体,经溶解、沉淀、过滤、干燥、称量等操作,其中沉淀需要洗涤,且要验证是否洗涤完全,向上层清液中继续滴加加氯化钡溶液,若有沉淀产生说明还没有沉淀完全,故答案为:称取样品;在上层清液中继续滴加加氯化钡溶液,观察有无沉淀产生.
点评 本题主要考察实验现象等观察、物质的提纯,中和滴定、实验过程设计及有关计算,题目难度不大,注意滴定管的使用,以及相对误差的计算方法.


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | OH-的物质的量相同 | B. | H+ 物质的量浓度相同 | ||
| C. | OH-的物质的量浓度不同 | D. | H+的物质的量浓度不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 操作 | 现象 | 结论 |
| A | 灼烧白色粉末,直接观察火焰颜色 | 火焰呈黄色 | 原粉末中有Na+无K+ |
| B | 将一块Al箔在酒精灯火焰上灼烧 | Al箔熔融而不滴落 | Al2O3具有较高的熔点 |
| C | 将一小块Na放入硫酸铜溶液中 | 有铜单质析出 | Na能置换出硫酸铜中的铜 |
| D | 将水蒸气通过灼热的铁粉 | 粉末变红 | 铁与水在高温下发生反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 往NaHC2O4溶液中通入氨气至中性:c(H2C2O4)+c(NH4+)>c(C2O42-) | |
| B. | 将pH=a的醋酸稀释为pH=a+1的过程中,c(CH3COOH)/c(H+)变小 | |
| C. | 常温下,将等体积、等物质的量浓度的NH4HCO3与NaCl溶液混合,析出部分NaHCO3晶体后过滤,所得滤液中存在:c(H+)+c(NH4+)=c(OH-)+c(HCO3-)+2c(CO32-) | |
| D. | 在同浓度的HCN和NaCN的混合溶液中,若pH>7,则c(HCN)<c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠与水的反应 | |
| B. | 灼热的炭与二氧化碳反应生成一氧化碳 | |
| C. | 高炉炼铁 | |
| D. | 氢氧化钠溶液与稀盐酸的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
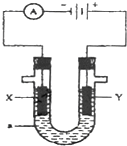 如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素B的单质与化合物A2D反应能生成D的单质 | |
| B. | 工业上利用铝热反应可制得单质C | |
| C. | 原子B、C、D半径的大小顺序:D>C>B | |
| D. | 一定条件下,过量的B单质与D单质直接生成BD3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com