
某溶液中除H+、OH-外,还含有大量的Mg2+、Fe3+、Cl-,且这三种离子物质的量浓度之比为1∶1∶6。下列有关该溶液的判断正确的是( )
A.向该溶液中加入KI溶液后,原有的五种离子物质的量不变
B.向该溶液中滴加稀氢氧化钠溶液,立即出现红褐色沉淀
C.若溶液中c(Cl-)=0.6 mol·L-1,则该溶液的pH为1
D.向该溶液中加入过量铁粉,只发生置换反应
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.有氧气参加的反应一定是燃烧
B.燃烧一定要有氧气参加
C.氢气在氯气中燃烧,火焰呈绿色
D.任何发光放热的剧烈的化学反应都可以叫燃烧
查看答案和解析>>
科目:高中化学 来源: 题型:
已检测出pH=1的某未知溶液中含有Al3+和NO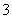 ,若检验此溶液中是否大量存在以下6种离子:①ClO- ②NH
,若检验此溶液中是否大量存在以下6种离子:①ClO- ②NH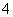 ③Fe2+④K+ ⑤HCO
③Fe2+④K+ ⑤HCO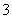 ⑥Cl-,其中不必检验就能加以否定的离子是( )
⑥Cl-,其中不必检验就能加以否定的离子是( )
A.①②⑥ B.②③④
C.①③⑤ D.④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是( )
A.利用醋酸溶解含碳酸钙的水垢:CaCO3+2H+===Ca2++H2O+CO2↑
B.用铜为电极电解饱和食盐水:2Cl-+2H2O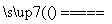 Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
C.在明矾溶液中滴加过量氨水:Al3++4NH3·H2O===AlO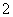 +4NH
+4NH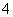 +2H2O
+2H2O
D.在小苏打溶液中加少量Ba(OH)2溶液:2HCO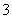 +Ba2++2OH-===BaCO3↓+2H2O+CO
+Ba2++2OH-===BaCO3↓+2H2O+CO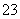 [来源:
[来源:
查看答案和解析>>
科目:高中化学 来源: 题型:
2012年3月21 日是第二十届“世界水日”,保护水资源,从我做起!
(1)ClO2和Cl2(还原产物都为Cl-)是生活中常用的消毒剂。当消耗等物质的量的两种物质时,ClO2的消毒效率是Cl2的________倍。
(2)某无色废水中可能含有Fe3+、Al3+、Mg2+、Na+、NO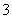 、CO
、CO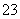 、SO
、SO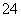 离子中的几种,为分析其成分,分别取废水样品100 mL,进行了三组实验,其操作和有关现象如下图所示:
离子中的几种,为分析其成分,分别取废水样品100 mL,进行了三组实验,其操作和有关现象如下图所示:
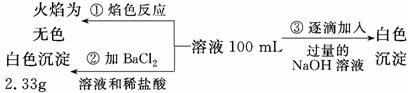
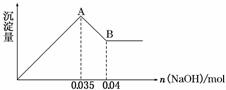
请根据上图回答下列问题:
①实验中需配制1.0 mol/L的NaOH溶液100 mL,所需仪器除了玻璃棒 、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器为_________________________________________。
、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器为_________________________________________。
②实验③中沉淀量由A→B过程中所发生反应的离子方程式为____________________。
③试确定NO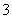 是否存在?________(填“存在”、“不存在”或“不确定”),若存在,试计算c(NO
是否存在?________(填“存在”、“不存在”或“不确定”),若存在,试计算c(NO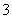 )=________(若不存在,此问不必作答)。
)=________(若不存在,此问不必作答)。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强,下列说法正确的是( )
A.化合物XZW既含离子键也含共价键
B.对应气态氢化物的稳定性Y>Z
C.对应简单离子半径:X>W
D.Y的氧化物能与Z或X的最高价氧化物对应的水化物反应
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:P4(g)+6Cl2(g)===4PCl3(g) ΔH=a kJ·mol-1,
P4(g)+10Cl2(g)===4PCl5(g) ΔH=b kJ·mol-1,
并知形成或拆开1 mol化学键放出或吸收的能量称为该化学键的键能。P4具有正四面体结构,PCl5中P-Cl键的键能为c kJ·mol-1,PCl3中P-Cl键的键能为1.2c kJ·mol-1。
下列叙述正确的是( )
A.P-P键的键能小于P-Cl键的键能
B.可求Cl2(g)+PCl3(g)===PCl5(s)的反应热ΔH
C.Cl-Cl键的键能为(b-a+5.6c)/4 kJ·mol-1
D.P-P键的键能为(5a-3b+12c)/8 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-、HCO3-等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀物质的量随NaOH溶液的体积变化的图象如图所示,下列说法正确的是( )
A.原溶液中含有的Fe3+和Al3+的物质的量之比为1:1
B.ab段发生的离子反应为:Al3++3OH-= Al(OH)3↓,Mg2++2OH-= Mg(OH)2↓
C.原溶液中含有的阳离子是H+、NH4+、Mg2+、Al3+、Na+
D.d点溶液中含有的溶质只有Na2SO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com