
| A. | SO2 | B. | CO2 | C. | NO | D. | NO2 |
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案科目:高中化学 来源: 题型:选择题
| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 |
| n(SO2)/mol | 0.20 | 0.16 | 0.13 | 0.11 | 0.08 | 0.08 |
| A. | 当容器中气体的密度不变时,该反应达到平衡状态 | |
| B. | 若要提高SO2的转化率,可用空气代替纯氧气并鼓入过量空气 | |
| C. | 从反应开始到达到平衡,用SO3表示的平均反应速率为0.01 mol/(L•min) | |
| D. | 容器内达到平衡状态时的压强与起始时的压强之比为5:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 非金属性强弱:I>Br>Cl | B. | 原子半径大小:Na>P>S | ||
| C. | 碱性强弱:KOH>NaOH>LiOH | D. | 金属性强弱:Na>Mg>Al |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NCl3 的沸点高于 NH3 的沸点 | |
| B. | 在氨水中,大部分 NH3 与 H2O 以氢键(用“…”表示)结合形成 NH3•H2O 分子,则NH3•H2O 的结构式为 | |
| C. | NCl3 分子是非极性分子 | |
| D. | NBr3 比 NCl3 易挥发 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
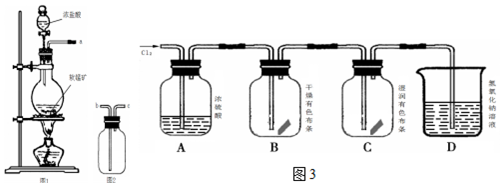
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献.
原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该变化一定是化学变化 | B. | 该变化一定伴随若能量的变化 | ||
| C. | 该变化一定有共价键的断裂与生成 | D. | 该变化一定有电子的转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将乙烯和甲烷分别通入酸性高锰酸钾溶液,观察溶液颜色是否变化 | |
| B. | 将溴水分别加入到四氯化碳和苯中,观察溶液颜色及是否分层 | |
| C. | 苯和己烷分别放入水中,观察液体是否分层 | |
| D. | 甲苯和硝基苯分别放入水中,观察液体是否分层 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠在反应TiCl4+4Na═Ti+4NaCl中作还原剂 | |
| B. | NaOH应密封保存,以防分解变质 | |
| C. | 盛放KOH溶液的试剂瓶不能用玻璃塞 | |
| D. | 当足量的CO2通入饱和NaOH溶液中,会有固体析出 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com