
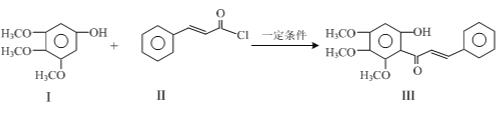
【题目】化合物Ⅲ是合成中药黄芩中的主要活性成分的中间体,合成方法如下:
 +HCl
+HCl
下列有关叙述正确的是
A.I的分子式为C9H10O4
B.II中所有原子有可能均共面
C.可用FeCl3溶液鉴别有机物I和III
D.1 mol产物III与足量溴水反应,消耗Br2的物质的量为1.5 mol
科目:高中化学 来源: 题型:
【题目】氰(CN)2的结构简式为N≡C—C≡N,其化学性质与卤素(X2)很相似,化学上称之为拟卤素,其氧化性介于Br2和I2之间。下列有关反应的化学方程式不正确的是( )
A. (CN)2+H2=2HCN
B. MnO2+4HCN=Mn(CN)2+(CN)2↑+2H2O
C. 向KCN溶液中加入碘水:I2+2KCN=2KI+(CN)2
D. 在NaBr和KCN混合液中通入少量Cl2:Cl2+2KCN=2KCl+(CN)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计的微型实验装置验证SO2的性质,通过分析实验,下列结论表达正确的是

A. a棉球褪色,验证SO2具有氧化性
B. b棉球褪色,验证SO2具有酸性氧化物的通性
C. c棉球蓝色褪去,验证SO2漂白性
D. 可以使用浓硫酸吸收尾气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲同学用图1所示实验装置测定锌与稀硫酸反应的速率
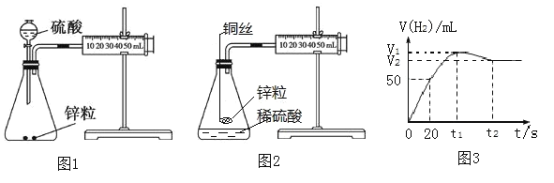
(1)甲同学测得产生H2体积与反应时间的关系如图3所示,该条件下气体摩尔体积为25 L·mol-1 ,溶液体积为40 mL,在20 s内用Zn2+浓度表示的平均反应速率v(Zn2+)=_____________mol·(L·s)-1。
(2)实际测定中发现在t1到t2时段,H2的体积变化如图3所示,试分析变化的原因:________
(3)乙同学认为图1装置中硫酸溶液的体积对H2的体积测定存在一定的影响 ,将实验装置进行如图2所示改进,结果发现产生氢气的速率发生明显变化,分析可能的原因________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在有机合成中官能团的引入或改变是极为重要的,下列说法正确的是( )
A.甲苯在光照下与Cl2反应,主反应为苯环上引入氯原子
B.引入羟基的方法常有卤代烃和酯的水解、烯烃的加成、醛类的还原
C.将CH2=CH—CH2OH与酸性KMnO4溶液反应即可得到CH2=CH—COOH
D.HC≡CH、(CN)2、CH3COOH三种单体在一定条件下发生加成、酯化反应即可得到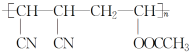
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据反应路线及所给信息填空。

(1)烃A的结构简式是___________,名称是___________________。
(2)①的反应类型是:_____________。③的反应类型是:______________。
(3)反应④的化学方程式是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用浓盐酸的质量分数为![]() ,密度为
,密度为![]() 。
。
(1)此盐酸的物质的量浓度为____________。
(2)需要![]() 的盐酸,配制时需以上浓盐酸的体积为_____
的盐酸,配制时需以上浓盐酸的体积为_____![]() 。
。
(3)上述实验中所用到的玻璃仪器有烧杯、玻璃棒、量筒以及____________(两种仪器)。
(4)用浓盐酸配制![]() 稀盐酸,操作步骤的正确顺序是__________(填字母代号)。
稀盐酸,操作步骤的正确顺序是__________(填字母代号)。
a.计算需要浓盐酸的体积
b.用量筒量取浓盐酸
c.将烧杯中的溶液注入所需容积的容量瓶中,并用少量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液也注入容量瓶
d.把量好体积的浓盐酸倒入烧杯中,加适量蒸馏水稀释,冷却
e.盖好瓶塞,反复上下颠倒,摇匀
f.继续向容量瓶中加蒸馏水至刻度线下1~2cm处,改用某仪器小心滴加蒸馏水至凹液面与刻度线相平
(5)下列操作使溶液物质的量浓度偏高的是:____________。
A.量取浓盐酸时仰视刻度线
B.容量瓶洗净后未经干燥处理
C.未冷却至室温就转移定容
D.没有将洗涤液转移到容量瓶中
E.定容时俯视刻度线
F.摇匀后立即观察,发现溶液未达到刻度线,再加几滴蒸馏水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)利用电化学原理将CO、SO2转化为重要化工原料,装置如图所示:
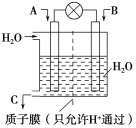
①若A为CO,B为H2,C为CH3OH,则通入CO的一极为___极,该极的电极反应式为___。
②若A为SO2,B为O2,C为H2SO4,则负极的电极反应式为___。
③若A为NH3,B为O2,C为HNO3,则正极的电极反应式为___。
④若用上述①作电池电解200mL含有0.1mol·L-1NaCl和0.1mol·L-1CuSO4的混合溶液(电极均为惰性电极),当消耗标况下0.448LH2时,阳极产生的气体为___(填化学式),其物质的量为___,溶液的pH=___(忽略铜离子水解,假设电解前后溶液体积不变)。
(2)根据2CrO42-+2H+![]() Cr2O72-+H2O设计图示装置(均为惰性电极)
Cr2O72-+H2O设计图示装置(均为惰性电极)
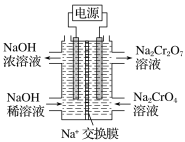
电解Na2CrO4溶液制取Na2Cr2O7,图中右侧电极连接电源的___极,其电极反应式为___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com