
在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),反应的化学方程式为 ,若反应中有0.3 mol电子发生转移时,生成亚硝酸的质量为 g(小数点后保留两位有效数字)。
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:
 活性炭吸附法是工业提碘的主要方法之一。其流程如下:
活性炭吸附法是工业提碘的主要方法之一。其流程如下:
完成下列填空:
28.酸性条件下,NaNO2溶液只能将 I-氧化为I2,同时生成NO。写出反应①的离子方程式并标出电子转移的数目和方向 。
29.氯气、浓硝酸、酸性高锰酸钾等都是常用的强氧化剂,但工业上氧化卤水中I-选择了价格并不便宜的亚硝酸钠,可能的原因是什么? 。
30.反应②发生时,溶液底部有紫黑色的固体生成,有时溶液上方产生紫色的气体。解释产生这种现象的原因 ,所以,反应②需要在 条件下进行。
31.流程中,碘元素经过了I2→I-、IO3-→I2的变化过程,这样反复的原因是 。
32.流程中用到的NaHSO3溶液显弱酸性。是因为该溶液中存在以下的平衡:
①HSO3– + H2O H2SO3 + OH– 和 ② (写出离子方程式)
H2SO3 + OH– 和 ② (写出离子方程式)
向0.1mol/L的NaHSO3溶液中分别加入以下物质,回答问题:
a.加入少量金属Na,平衡①如何移动? 溶液的pH如何变化?
b.加入氨水至中性,则式子:c(Na+) = c(SO32–)+ c(HSO3–)+ c(H2SO3)>c(H+) = c(OH–),是否正确 ,解释原因 。
查看答案和解析>>
科目:高中化学 来源: 题型:
硝酸铵是一种常用的化肥,其工业生产流程如下图,请回答下列问题。
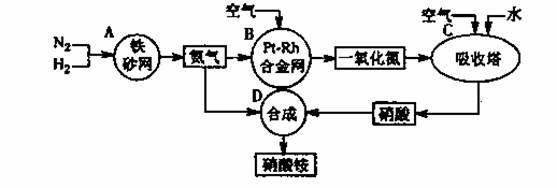
⑴写出反应容器B中发生反应的化学方程式: 。
⑵吸收塔C中通入空气的目的是 ;C、D两个反应容器中发生的反应,属于氧化还原反应的是 (填反应容器代号)。
⑶浓硝酸一般保存在棕色试剂瓶里,并放置在阴凉处,用化学方程式解释原因: 。
⑷金属铜与稀硝酸反应的离子方程式是 ,该反应中稀硝酸表现的性质是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验表述正确的是
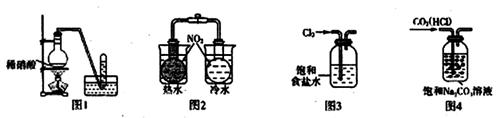
A.图l:用于制取纯净的NO2气体 B.图2:用于研究温度对化学平衡的影响
C.图3:用于实验室Cl2的收集 D.图4:用于除去CO2气体中的HCl杂质
查看答案和解析>>
科目:高中化学 来源: 题型:
有温度、容积相同的甲、乙两个密闭容器。往甲容器中通入1g N2和1g H2,乙容器中通入2g N2和2g H2,保持恒温、恒容达到平衡,相关参数比较正确的是
A.平衡时N2的转化率:α甲>2α乙 B.平衡时NH3的浓度:2c甲<c乙
C.平衡时体系压强:2p甲>p乙 D.反应放出的热量:2Q甲>Q
查看答案和解析>>
科目:高中化学 来源: 题型:
以电石渣(主要成分是Ca(OH)2,含SiO2以及其它少量杂质)为原料生产氯酸钾联合生产碳酸钙的流程如下:

回答下列问题:
电石渣溶于水形成电石渣浆时发生的主要反应的化学方程式为: 氯化过程的温度控制在75~80℃,该过程主要反应的离子方程式为: _______________________________________________________________ 该流程中加入活性炭的作用是
碳化过程中,先向溶液中通入氨气,再通入CO2。
①实验室通常采用加热氯化铵和氢氧化钙混合物的方法制取氨气。某学习小组选取下图所给部分装置制取并收集纯净的氨气。
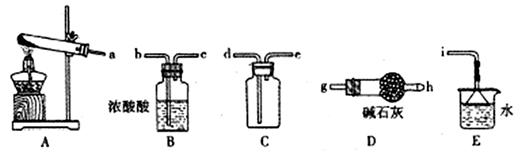
如果按气流方向连接各仪器接口,你认为正确的顺序为a→ 、 → 、 →i。其中与i相连漏斗的作用是 。
②实验室中还可用固体氢氧化钠和浓氨水制取少量氨气,下列最适合完成该实验的简易装置是 (填编号)
 副产品A的化学式为 。
副产品A的化学式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
工业生产水煤气的反应为:C(s)+H2O(g)=CO(g)+H2(g) ΔH= +131.4 kJ/mol,下列判断正确的是
A.水煤气反应中生成1 mol H2(g)吸收131.4 KJ热量
C.反应物能量总和大于生成物能量总和
B.CO(g)+H2(g)=C(s)+H2O(l) ΔH= -131.4 kJ/mol
D.水煤气反应中生成1体积CO(g)吸收131.4 KJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定体积的密闭容器中,进行如下化学反应:
CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应为 反应(选填“吸热”、“放热”),该反应平衡常数表达式为 ;
(2)830℃时,容器中的反应已达到平衡。在其他条件不变的情况下,扩大容器的体积。平衡 移动(选填“向正反应方向”、“向逆反应方向”、“不”)。
(3)若 830℃时,向容器中充入1mol CO、5mol H2O,反应达到平衡后,其化学平衡常数K 1.0(选填“大于”、“小于”、“等于”)
(4)若1200℃时,在某时刻平衡体系中CO2、H2、CO、H2O的浓度分别为2 mol·L-1、
2 mol·L-1、4 mol·L-1、4 mol·L-1,则此时上述反应的平衡移动方向为 。(选填“正反应方向”、“逆反应方向”、“不移动”)
查看答案和解析>>
科目:高中化学 来源: 题型:
减小压强时,对已达化学平衡的反应2X(g)+Y(g)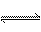 2Z(g)产生的影响是
2Z(g)产生的影响是
A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动
B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动
C.正、逆反应速率都减小,平衡向逆反应方向移动
D.正、逆反应速率都增大,平衡向正反应方向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com