
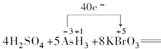 ,故答案为:
,故答案为: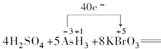 .
.


科目:高中化学 来源: 题型:
| A、向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| B、物质的量浓度相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液中c(NH4+):(NH4)2SO4>NH4HSO4>NH4Cl |
| C、1.0mol/L Na2CO3溶液:c(OH-)=2c(HCO3-)+c(H+)+c(H2CO3) |
| D、某二元弱酸的酸式盐NaHA溶液中:c(H+)+c(Na+)=c(OH-)+c(HA-)+c(A2-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe3+、H+、SO42-、ClO- |
| B、K+、H+、I-、MnO4- |
| C、Al3+、Na+、SO42-、CO32- |
| D、Fe3+、Fe2+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| O | 2- 4 |
| O | 2- 4 |
| A、3:2 | B、3:4 |
| C、1:2 | D、1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子数 | B、分子数 |
| C、体积 | D、物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
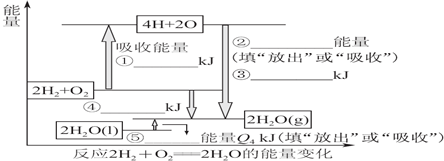
查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间/min | CO | H2O(g) | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
| 5 | 0.116 | 0.216 | 0.084 | C1 |
| 6 | 0.096 | 0.266 | 0.104 | C2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验步骤 | 实验现象 | 结论 | |
| ① | 取少量上述漂白粉于试管中,加入适量1mol/L盐酸溶解后,再将产生的气体导入到澄清石灰水中 | 石灰水变浑浊 | |
| ② | 向上述反应后的试管滴入1~2滴品红溶液,振荡 | 品红褪色 | |
| 实验内容 | 将氯气持续通入淀粉碘化钾溶液 |
| 实验现象 | 溶液先变蓝,后褪色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com