
【题目】钛的化合物如TiSe2、Ti(NO3)4、TiCl4、酒石酸钛等均有着广泛用途。

(1)写出Se的基态原子的外围电子排布式 。
(2)酒石酸钛配合物广泛应用于药物合成。酒石酸(结构如下图所示)中羧基氧原子的轨道杂化类型分别是 ,1 mol酒石酸中π键的数目是 。
(3)TiCl4熔点是—25℃,沸点136.4℃,可溶于苯或CCl4,该晶体属于 晶体;
NO3-离子的空间构型为 。
(4)主族元素A和钛同周期,具有相同的最外层电子数,元素B原子的p能级所含电子总数与s能级所含电子总数相等,且其形成的氢化物分子之间存在氢键。元素A、元素B和钛三者形成的晶体的晶胞如图所示,写出该晶体的化学式 (用元素符号表示)。
【答案】(1)4s24p4 (2)sp3和 sp2 2mol(3)平面三角形(4)CaTiO3
【解析】
试题分析:(1)Se的原子核外有34个电子,最外层有6个电子,则其核外电子分4层排布,最外层为电子排布为4s24p4;
(2)羧基的结构式为 ,两个O原子的价层电子对数分别为3、4,则杂化类型分别为sp2、sp3;酒石酸分子中含有2个羧基,每个羧基含有一个C=O,双键中含有一个π键,则一分子酒石酸中含有2个π键,则1mol酒石酸中π键的数目是2NA;
,两个O原子的价层电子对数分别为3、4,则杂化类型分别为sp2、sp3;酒石酸分子中含有2个羧基,每个羧基含有一个C=O,双键中含有一个π键,则一分子酒石酸中含有2个π键,则1mol酒石酸中π键的数目是2NA;
(3)由于TiCl4熔点是-25℃,沸点136.4℃,可溶于苯或CCl4,分子晶体的熔沸点较低,所以TiCl4属于分子晶体;NO3-中N原子的价层电子对数=3+1/2(5+1-3×2)=3,属于sp2杂化,没有孤电子对,所以NO3-的构型为平面三角形;
(4)主族元素A和钛同周期,具有相同的最外层电子数,则最外层含有2个电子,A为Ca元素,元素B原子的p能级所含电子总数与s能级所含电子总数相等,且其形成的氢化物分子之间存在氢键,已知N、O、F的氢化物能形成氢键,则B为O,Ca占据晶胞的顶点,则晶胞中Ca的个数为1/8×8=1,O占据面心,则晶胞中O原子的个数为1/2×6=3,Ti在晶胞内部,完全属于该晶胞,则该晶体的化学式CaTiO3。


科目:高中化学 来源: 题型:
【题目】A,B,C,D,E代表5种元素。请按要求填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为__________;其价层电子排布图为________。
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B的元素原子的名称为________,C离子的结构示意图为____________________________。
(3)D元素的正三价离子的3d能级为半充满,D的元素符号为________,其基态原子的电子排布式为____________________,其原子的结构示意图为______________。
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为________,其基态原子价层电子排布式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组为探究草酸的性质并制备草酸钠及其用途,查阅到如下信息:

探究草酸部分性质并制备草酸钠的生产流程如下:
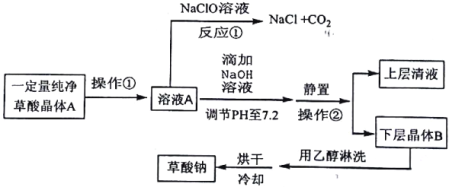
请回答下列问题:
(1)写出反应①的化学方程式__________。表明草酸具有__________性。
(2)向溶液A中加入NaOH溶液,开始滴加速度要尽量快些.其目的是__________。该反应达到终点时的化学方程式为__________。
(3)操作②的名称是__________。用乙醇淋洗晶体B的目的是__________
(4)用0.01000mol/L的高锰酸钾溶液滴定25.00mL某浓度的草酸钠溶液时.需要加入适量的稀硫酸,所发生反应为:5C2O42-+2MnO4-+16H+=2Mn2++10CO2↑+8H2O,若硫酸加入太多,结果会__________:操作中需用__________滴定管(填“酸式”或“碱式”),当达到反应终点时的现象是__________;测得此时消耗上述高锰酸钾溶液20.00mL,则该草酸钠溶液浓度为__________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.根据反应Fe+H2SO4=FeSO4+ H2↑ 回答下列问题。
(1)在此反应中,自反应开始至2分钟末,H2SO4浓度由1mol/L变为0.4mol/L,则H2SO4的反应速率为 。若要使该反应的反应速率加快,下列措施不可行的是 (填字母)
a、改铁片为铁粉 b、改稀H2SO4为98%的浓H2SO4
c、升高温度 d、滴加少量CuSO4溶液
(2)在答题卡的坐标图中,画出此反应过程中体系的能量变化图(进行必要的标注)
(3)根据此反应设计一个原电池,要求画出装置图并进行必要的标注
Ⅱ.某校化学兴趣小组设计了图示实验装置(图中省略了夹持仪器)来测定某铁碳合金中铁的质量分数。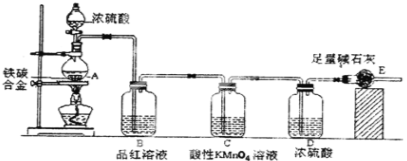
(1)将a g铁碳合金样品放入装置A中,再加入足量的浓硫酸,加热,待A中不再逸出气体时,停止加热,拆下E并称重,E增重b g。铁碳合金中铁的质量分数为____________(写表达式)。
(2)反应一段时间后,从A中逸出气体的速率仍然较快,除因温度较高,反应放热外,还可能的原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。
请回答:
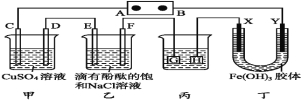
(1)B极是电源的 ,一段时间后,甲中溶液颜色 ,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明 在电场作用下向Y极移动。
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为 。
(3)现用丙装置给铜件镀银,则H应是 ,电镀液是 溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[有机化学基础] 有机物H是一种重要的医药中间体。其结构简式如图所示:
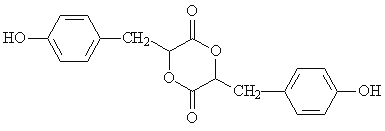
合成H的一种路线如下:
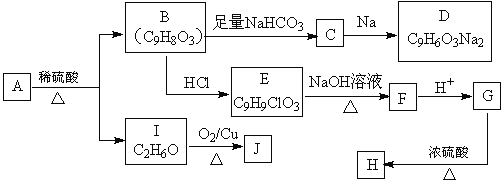
已知以下信息:
①有机物A遇氯化铁溶液发生显色反应,其分子中的苯环上有2个取代基,且A的苯环上一氯代物有2种。 ②J能发生银镜反应。
请回答下列问题:
(1)I的名称是 。G生成H的反应类型是 。
(2)B的含氧官能团名称是 ;E生成F的化学方程式为 。
(3)在一定条件下,A与J以物质的量比1∶1反应生成功能高分子材料K,K的结构简式为 。
(4)已知:![]() ,C与E以物质的量比1∶1混合在催化剂、加热条件下反应,写出化学方程式 。
,C与E以物质的量比1∶1混合在催化剂、加热条件下反应,写出化学方程式 。
(5)L是B的同分异构体,L符合下列条件的结构有 种(不考虑立体结构)。
①与B具有相同的官能团;②遇氯化铁溶液发生显色反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用甲烷与氯气发生反应制取盐酸的设想,在工业上已成为现实。某化学兴趣小组拟在实验室中模拟上述过程,其设计的模拟装置如下:
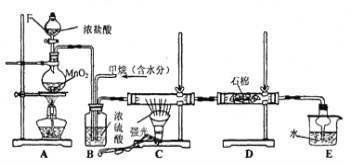
根据要求填空:
(1)装置A中反应的离子方程式为 ;
(2)B装置有三种功能:
①控制气流速度;② ;③ 。
(3)在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,写出置换出黑色小颗粒的化学方程式 。
(4)D装置中的石棉上均匀附着湿润的KI粉末,其作用是 ,
E装置的作用是 。
(5)装置中除了有盐酸生成外,还含有有机物,从E中分离出盐酸的最佳方法为 ;
该装置还有缺陷,原因是没有进行尾气处理,写出尾气中的主要成分是 。
(填编号)
A.CH4 B.CH3Cl C.CH2Cl2 D.CHCl3 E.CCl4
(6)实验之余,该学习小组进一步探究甲烷与氯气反应的条件。

通过排饱和食盐水的方法收集两瓶甲烷与氯气(体积比为1∶4)混合气体(I、II),II瓶用预先准备好的黑色纸套套上,I瓶放在光亮处(不要放在日光直射的地方,以免引起爆炸)。按上图安装好装置,并夹紧弹簧夹a和b。过一段时间,打开弹簧夹a、b,I、II中观察到现象是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某种烷烃A在同温同压下蒸气的密度是H2的43倍, 则该烃的分子式 。
(2)某烷烃B含有16个共价键,则该烃的同分异构体有 种。
(3)某烷烃C的结构简式为CH3CH2CH(CH3)2,则该烃的一氯取代物有 种。
(4)某烃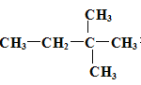 由另一种烃D通过加成反应而制得,则烃D的可能的是 (任写一种可能的结构简式)。
由另一种烃D通过加成反应而制得,则烃D的可能的是 (任写一种可能的结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷(As)是第四周期第VA族元素,它在自然界中的含量不高,但人类认识它、研究它的历史却很长。
(1)砷的氢化物的化学式为________,其稳定性比磷的氢化物____(填“强或弱”)。已知H3AsO3是两性偏酸性的化合物,它与硫酸反应的化学方程式为 。NaHAsO3溶液呈碱性,该溶液中c(H2AsO3-) C(AsO33-)(填“>”、“<”或“=”)。
(2)砷在自然界中主要以硫化物形式(如雄黄As4S4、雌黄As2S3等)存在。
①工业上以雄黄为原料制备砷的过程是:先在空气中煅烧使其转化为砒霜(As2O3),然后用焦炭还原。写出焦炭还原时发生反应的化学方程式: 。砒霜有剧毒,卫生防疫分析中鉴定的方法是:先将试样与锌、硫酸混合在一起反应,将生成的气体导入到热玻璃管中热解,若玻璃管中产生亮黑色的“砷镜”,则说明试样中含有As2O3。写出上述鉴定过程中有关反应的化学方式: 。
②“砷镜”可被漂白精氧化为H3AsO4,反应中还原剂与氧化剂物质的量之比为 。
(3)已知砷酸(H3AsO4)是三元酸,有较强的氧化性。
①常温下砷酸的K1=6×10-3、K2=1×10-7,则NaH2AsO4溶液的pH为____7。(填“>”、“<”、“=”),判断依据为___________________________________________________________________。
②某原电池装置如图所示,电池总反应为AsO43-+2I-+H2O![]() AsO33-+I2+2OH-。
AsO33-+I2+2OH-。
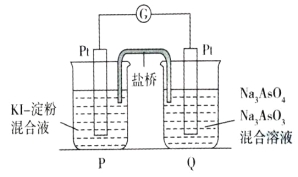
当P池中溶液由无色变成蓝色时,正极上的电极反应式为 。当电流计指针归中后向Q池中加入一定量的NaOH,则电池负极所在的烧杯为 (填“P”或“Q”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com