
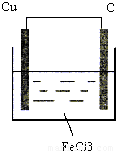
 ,负极(Cu):Cu-2e-=Cu2+,正极(C):2Fe3++2e-=2Fe2+.
,负极(Cu):Cu-2e-=Cu2+,正极(C):2Fe3++2e-=2Fe2+.

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)如图所示装置:①若烧杯中溶液为稀硫酸,则观察到的现象为
(1)如图所示装置:①若烧杯中溶液为稀硫酸,则观察到的现象为查看答案和解析>>
科目:高中化学 来源:2010—2011学年江西省德兴一中高一下学期第一次月考化学试卷 题型:填空题
(6分)利用Cu + 2FeCl3 = CuCl2 + 2FeCl2反应,设计一个原电池。
(1)画出装置图(在图中标出电极材料、正负极、电解质溶液)。(2分)
(2)写出电极反应方程式
负极 :
:
正极: (各2分)
查看答案和解析>>
科目:高中化学 来源:2013届江苏省姜堰市高一下学期期中考试化学试卷 题型:填空题
(6分)利用Cu + 2FeCl3 = CuCl2 + 2FeCl2反应,设计一个原电池,写出电极反应式。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com