
| A. | 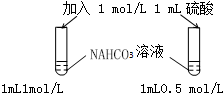 探究浓度对化学反应速率的影响 | B. | 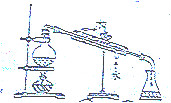 分离乙醇和乙酸的混合溶液 | ||
| C. | 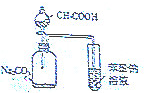 证明酸性:CH3COOH>H2CO3>苯酚 | D. | 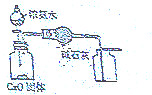 制取并且收集干燥纯净的NH3 |
分析 A.只有碳酸氢钠的浓度不同;
B.乙醇和乙酸的混合溶液不分层,沸点不同;
C.醋酸易挥发,醋酸也与苯酚钠反应生成苯酚;
D.氨气的密度比空气小,利用向下排空气法收集.
解答 解:A.只有碳酸氢钠的浓度不同,只有一个变量,则该实验可探究浓度对化学反应速率的影响,浓度大生成气体的速率快,故A正确;
B.乙醇和乙酸的混合溶液不分层,沸点不同,可利用图中蒸馏装置分离,且冷水下进上出,故B正确;
C.醋酸易挥发,醋酸也与苯酚钠反应生成苯酚,则不能比较醋酸、苯酚的酸性,故C错误;
D.氨气的密度比空气小,利用向下排空气法收集,则图中氨气的收集方法不合理,故D错误;
故选AB.
点评 本题考查化学实验方案的评价,为高频考点,涉及影响反应速率的因素、混合物分离提纯、酸性比较、气体的制备及收集等,把握物质的性质、反应原理为解答的关键,侧重分析与实验能力的考查,注意实验装置的作用及实验评价性分析,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
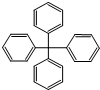
| A. | 分子式为C25H20 | |
| B. | 分子中所有原子有可能处于同一平面 | |
| C. | 该化合物分子中所有原子不可能处于同一平面 | |
| D. | 分子中处于同一平面的原子最多23个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2S2O3溶液中加入稀硫酸的离子方程式为:2S2+4H+═SO42-+3S↓+2H2O | |
| B. | 用TiCl4制备TiO2的反应可表示为:TiCl4+(x+2)H2O(过量)═TiO2•xH2O↓+4HCl | |
| C. | 滴加甲基橙试液后呈红色的溶液中可以大量共存:Na+、CO32-、K+、Al3+ | |
| D. | 25℃时,pH=12的NaOH溶液中含有OH-的数目为0.01NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 431 kJ•mol-1 | B. | 945.6 kJ•mol-1 | C. | 649 kJ•mol-1 | D. | 896 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
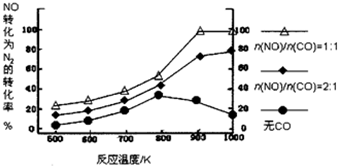
| A. | CO对NO转化为N2起抑制作用 | |
| B. | CO的催化效果随温度升高而提高 | |
| C. | NO的分解反应为放热反应 | |
| D. | $\frac{n(NO)}{n(CO)}$=1时,应控制的最佳温度在1000K |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第ⅠA族元素的金属性比第ⅡA族元素的金属性强 | |
| B. | 可以在元素周期表中金属与非金属元素分界线附近寻找合适的半导体材料 | |
| C. | 同周期非金属氧化物对应的水化物的酸性从左到右依次增强 | |
| D. | 第三周期元素的离子半径从左到右逐渐减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com