
| A. |  图所示的反应为放热反应 | |
| B. | 化学反应中有物质变化也有能量变化 | |
| C. | 需要加热的化学反应不一定是吸热反应 | |
| D. | 化学键断裂吸收能量,化学键生成放出能量 |
分析 A.根据图示中反应物与生成物能量高低进行判断;
B.化学反应一定有新物质的生成,同时一定伴随着能量变化;
C.很多放热反应,需要点燃或者加热才能使反应进行,溶液氧气与氢气的反应为放热反应,该反应需要点燃才能进行;
D.化学反应中,旧的化学键断裂需要吸收能量,新的化学键生成过程中会放出能量.
解答 解:A.由图示可知,在反应过程中,反应物总能量小于生成物总能量,该反应一定为吸热反应,故A错误;
B.有新的物质生成的反应为化学反应,所以化学反应一定有物质变化,并且反应过程中一定伴随着能量变化,通常以热量的形式释放出来,故B正确;
C.吸热反应不一定需要加热才能进行,如氢氧化钡晶体与氯化铵的反应;加热条件下能够进行的反应不一定为吸热反应,反应吸热还是放热与反应物和生成物总能量大小有关,与反应条件没有必然关系,故正确;
D.化学反应中,旧的化学键断裂需要吸收能量,新的化学键生成会放出能量,所以化学反应中一定伴随着能量变化,故D正确;
故选A.
点评 本题考查了化学反应与能量变化,题目难度不大,注意明确化学反应的实质,任何化学反应中一定伴随着能量变化,还要明确放热反应、吸热反应与反应条件没有必然关系.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 醋酸与烧碱混合:H++OH-═H2O | |
| B. | 大理石中加入盐酸:CO32-+2H+═CO2↑+H2O | |
| C. | 稀硫酸滴在铁片上:Fe+2H+═Fe2++H2↑ | |
| D. | 硫酸铜溶液和氢氧化钡溶液混合:Cu2++2OH-═Cu(OH)2↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氨燃料电池在放电时,氨气被氧化 | |
| B. | 氨燃料电池在放电时,正极反应为:2NH3+6e-+6OH-=N2+6H2O | |
| C. | 以氨气代替氢气的主要原因是:氨气易液化易储存 | |
| D. | 氨燃料电池产物为无污染的氮气和水,属于环境友好电池 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 叙述 | 评价 |
| A | 可用氢氧化钠醇溶液与硝酸酸化的硝酸银溶液鉴别烷烃与卤代烃 | 对.卤代烃都能与氢氧化钠醇溶液共热生成卤化钠.卤化钠与硝酸酸化的硝酸银溶液反应可生成卤化银沉淀 |
| B | 乙酸乙酯在H218O中水解,产物乙酸中将含有18O | 错,根据酯的水解规律,产物乙酸中将含有18O同位素.而乙醇則没有 |
| C | 不能用酸性高锰酸钾溶液除去甲烷中的乙烯气体 | 对.乙烯虽能与酸性高锰酸钾溶液反应,但会生成 CO2 |
| D | 可以用新制的Cu(OH)2悬浊液鉴别乙醇溶液、乙酸溶液和乙醛溶液 | 对.乙醇、乙酸和乙醛与新制的Cu(OH)2悬浊液反应现象皆不同.可以一次性鉴别 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 6种相邻短周期主族元素的相对位置如下表,M元素原子核外电子数是Y元素原子核外电子数的2倍,W元素原子的次外层电子数是最外层电子数的2倍.用化学用语回答下列问题:
6种相邻短周期主族元素的相对位置如下表,M元素原子核外电子数是Y元素原子核外电子数的2倍,W元素原子的次外层电子数是最外层电子数的2倍.用化学用语回答下列问题:| X | Y | Z | |
| W | M | Q |
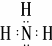 ,实验室制备甲的化学方程式是2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,甲可以与X的最高价氧化物对应的水化物溶液反应生成盐乙,乙溶液中的离子浓度由大到小的顺序是c(NO3-)>c(NH4+)>c(H+)>c(OH-).X的含18个电子的气态氢化物丙可与空气构成一种环保型碱性燃料电池,电池工作时丙发生的电极反应方程式是N2H4-4e-+4OH-═N2+4H2O.
,实验室制备甲的化学方程式是2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,甲可以与X的最高价氧化物对应的水化物溶液反应生成盐乙,乙溶液中的离子浓度由大到小的顺序是c(NO3-)>c(NH4+)>c(H+)>c(OH-).X的含18个电子的气态氢化物丙可与空气构成一种环保型碱性燃料电池,电池工作时丙发生的电极反应方程式是N2H4-4e-+4OH-═N2+4H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
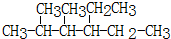 2,3-二甲基-3-乙基己烷
2,3-二甲基-3-乙基己烷 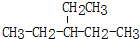 2-乙基戊烷
2-乙基戊烷查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com