
【题目】用下列实验装置进行相应实验,装置正确且能达到实验目的的是
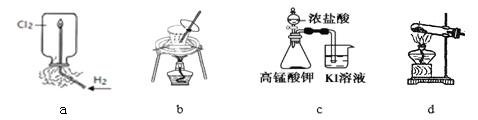
A. 用图a所示装置验证H2在Cl2中燃烧的实验现象
B. 用图b所示装置从饱和食盐水中提取氯化钠
C. 用图c所示装置探究氧化性:KMnO4>Cl2>I2
D. 用图d所示装置分解MgCl2·6H2O获取MgCl2
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(有毒性,市场上很易与食盐混淆)是一种常见的工业用盐,广泛用于物质合成、金属表面处理等,它的性质或用途,其物理性质与NaCl极为相似.相关化学性质如图所示,下列说法不正确的是( )
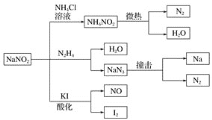
A. NaNO2稳定性大于NH4NO2 B. NaNO2与N2H4反应中,NaNO2是氧化剂
C. 可用KI淀粉和食醋鉴别NaNO2和NaCl D. 分解NaN3盐每产生1mol N2转移6mole-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是原子序数依次增大的常见短周期元素,X的某种氢化物能使湿润的红色石蕊试纸变蓝.Y的一种核素质量数为18,中子数为10.在同周期元素中Z的简单离子半径最小,W的单质是良好的半导体材料。下列说法中正确的是
A. 简单气态氢化物稳定性:W >X
B. Y元素的相对原子质量为18
C. X2H4的分子中极性键和非极性键数目比为4:l
D. 电解Z的熔融氯化物可以冶炼单质Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z,原子半径依次增大。W、X在同一主族,Y元素在第三周期中离子半径最小,Y和Z的原子序数之和是W的3倍。下列说法正确的是
A. X的简单氢化物的热稳定性比W的强 B. X的氧化物对应的水化物是强酸
C. Z和W形成的化合物可能含有非极性键 D. Z、Y的氧化物是常用的耐火材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关从海带中提取碘的实验原理和装置能达到实验目的的是
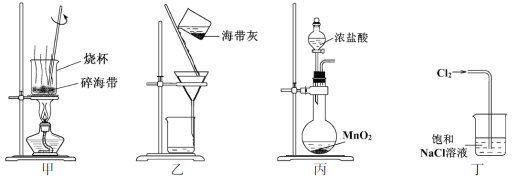
A. 用装置甲灼烧碎海带
B. 用装置乙过滤海带灰的浸泡液
C. 用装置丙制备用于氧化浸泡液中I的Cl2
D. 用装置丁吸收氧化浸泡液中I后的Cl2尾气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z和W代表原子序数依次增大的四种短周期主族元素.它们满足以下条件:①在元素周期表中,Z与Y、W均相邻;②X、Y、W分别位于不同周期;③Y、Z、W三种元素的原子最外层电子数之和为17。下列说法错误的是
A. X、Y、Z既能形成离子化合物,又能形成共价化合物
B. Y和Z元素的原子半径大小顺序为Y>Z
C. X与Y、Z之间形成的核外电子总数为10的微粒只有YX3和X2Z
D. Z、W元素的最简单氢化物的沸点和稳定性均为H2Z>H2W
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学探究学习小组拟利用如图所示装置(部分固定装置已略去)测定某黑色铜硫化物样品的化学式,按照如下步骤进行了实验。
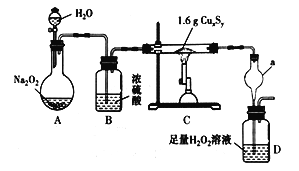
步骤一:利用右图所示装置,高温灼烧1.6gCuxSy至固体质量不再变化,得到红色固体和一种能使品红 溶液褪色的气体。
步骤二:将D中所得溶液按下述流程进行处理。
煮沸D中溶液并冷却→配制250mL溶液→取25.00mL溶液,滴入2-3滴酚酞溶液→滴定,消耗0.1 molL-1NaOH溶液20.00mL。
请回答下列问题:
(1)A装置中发生反应的化学方程式为_______________________。停止加热后还需继续通入一段时间的O2,其目的是________________________。
(2)仪器a的作用为________________。装置D中反应的化学方程式为__________________________。
(3)步骤二中配制溶液时所需的玻璃仪器除玻璃棒和烧杯外,还有___________;判断滴定终点的现象是____________________________。
(4)利用题中提供的数据可计算得出该铜硫化物的化学式为_______________。
(5)有同学认为可将装置D改为装有足量碱石灰的干燥管,通过测定反应前后干燥管的增重来计算硫元素的含量。你认为此方案(填“合理”或“不合理”),原因是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以铬铁矿(主要成分为FeOCr2O3)、碳酸钠、氧气、和硫酸为原料生产重铬酸钠(Na2Cr2O72H2O),其主要反应为:
(1)4FeOCr2O3+8Na2CO3+7O2![]() 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2
(2)2Na2CrO4+H2SO4![]() Na2SO4+Na2Cr2O7+H2O
Na2SO4+Na2Cr2O7+H2O
下列说法正确的是( )
A. 反应(1)和(2)均为氧化还原反应
B. 反应(1)的氧化剂是O2,还原剂是FeOCr2O3
C. 高温下,O2的氧化性强于Fe2O3,弱于Na2CrO4
D. 反应(1)中每生成1molNa2CrO4时电子转移3mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素X的某一个原子形成的离子可表示为![]() Xn-,下列说法正确的是( )
Xn-,下列说法正确的是( )
A. ![]() Xn-含有的中子数为a+bB. 这个X原子的质量约为
Xn-含有的中子数为a+bB. 这个X原子的质量约为![]() g
g
C. X元素的相对分子质量为bD. ![]() Xn-含有的电子数为a-n
Xn-含有的电子数为a-n
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com