
取代反应是有机化学中一类重要的反应,下列反应属于取代反应的是( )
A.丙烷与氯气在光照的作用下的反应 B.乙烯与溴的四氯化溶液的反应
C.乙烯与水的反应 D.乙烯自身生成聚乙烯的反应
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
某温度时,在1.0 L密闭容器内加入 2.0 mo1 SO2和1.0 mo1 O2,发生反应:
2SO2 (g) + O2 (g) 2SO3 (g)
请回答:
(1)反应进行2 min后,测得SO2 为1.4 mol,则2 min内
v(SO3) = mol/(L·min)。
(2)若升高温度能使化学平衡向逆反应方向移动,则正反应是 (填“放热”或“吸热”)反应。
(3)反应进行8 min后达平衡,测得c(SO3) = 8c(O2),则 SO2的平衡转化率是 。
(4)该温度下,此反应的平衡常数K的表达式为
在该温度下K的数值是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:2Fe+3Cl2 2FeCl3,下列说法正确的是(设NA为阿伏加德罗常数的值)
2FeCl3,下列说法正确的是(设NA为阿伏加德罗常数的值)
A.氯气是氧化剂,FeCl3是还原剂
B.常温下,与56g Fe反应断裂1.5NA个Cl-Cl键
C.1 L 0.1 mol·L-1 FeCl3溶液中含有0.1NA个Fe3+
D.常温常压下,22.4 L Cl2和足量Fe反应转移3NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
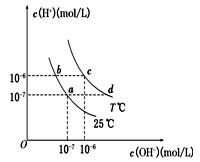
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系。下列条件关于离子共存说法中正确的是
A.d点对应的溶液中大量存在:Na+、K+、ClO-、Cl—
B.b点对应的溶液中大量存在:Fe2+、Ba2+、K+、NO3-
C.c点对应的溶液中大量存在:Na+、Ba2+、Cl-、Al3+
D.a点对应的溶液中大量存在:CO32-、Na+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
现有浓度均为0.1 mol·L-1的下列溶液:①硫酸 ②醋酸 ③氢氧化钠 ④氯化铵
请回答下列问题:
(1)四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)_____________________ _____________________________________。
(2)将③和④等体积混合后,混合液中各离子浓度由大到小的顺序是__________________________________________________。
(3)已知T ℃,KW=1×10-13,则T ℃________25 ℃(填“>”、“<”或“=”)。在T ℃时将pH=11的NaOH溶液a L与pH=1的硫酸b L混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=10,则a∶b=________。
(4)25 ℃时,有pH=x的盐酸和pH=y的氢氧化钠溶液(x≤6,y≥8),取a L该盐酸与b L该氢氧化钠溶液反应,恰好完全中和,求:
①若x+y=14,则a/b=________(填数据);
②若x+y=13,则a/b=________(填数据);
③若x+y>14,则a/b=________(填表达式);
④该盐酸与该氢氧化钠溶液完全中和,两溶液的pH(x、y)的关系式为________(填表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
50℃和1.01×105 Pa时,该反应能自发进行:2N2O5(g) = 4NO2(g) + O2(g) △H= +56.76 kJ/mol,其自发进行的原因是( )
A.是吸热反应
B.是放热反应
C.是熵减少的反应
D.熵增大效应大于能量效应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com