
分析 (1)具有相同质子数、不同中子数的原子,互为同位素;
(2)同种元素的不同单质,互为同素异形体;
(3)分子式相同、结构不同的有机物,互为同分异构体;
(4)结构相似,组成相差n个CH2原子团的有机物互为同系物,官能团的数目、种类应相同.
解答 解:(1)只有①11H 与 13H 符合具有相同质子数、不同中子数的原子,互为同位素,故答案为:①;
(2)只有②O2与O3 ⑥C60与C70符合同种元素的不同单质,互为同素异形体,故答案为:②⑥;
(3)只有③乙醇与甲醚(CH3-O-CH3)符合分子式相同、结构不同的有机物,互为同分异构体,故答案为:③;
(4)只有⑤均为烷烃,符合结构相似,组成相差n个CH2原子团的有机物,二者互为同系物,故答案为:⑤;
故答案为:①;②⑥;③;⑤.
点评 本题考查同位素、同系物、同分异构体的概念与辨析,题目难度不大,注意把握概念的内涵与外延.


科目:高中化学 来源: 题型:解答题
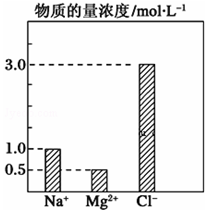 在0.2L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题:
在0.2L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 得电子越多,其氧化性越强 | B. | 分子中一定含有氧元素 | ||
| C. | 在反应中易失电子的物质 | D. | 在反应中易结合电子的物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KI的酸性溶液长期置于空气中:4I-+2H2O+O2═2I2+4OH- | |
| B. | 高锰酸钾酸性溶液与草酸溶液反应:2MnO4-+5C2O42-+16H+═2Mn2++10CO2↑+8H2O | |
| C. | 用稀硫酸除去铁片表面的铁锈:FeO+2H+═Fe2++H2O | |
| D. | 硫代硫酸钠溶液中滴加稀硫酸:2H++S2O32-═S↓+SO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
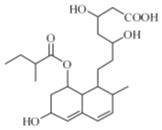
| A. | 能与FeCl3 溶液发生显色反应 | |
| B. | 能使酸性KMnO4 溶液褪色 | |
| C. | 能发生加成、取代、消去反应 | |
| D. | 1mol该物质最多可消耗4molNaOH、2molBr2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com