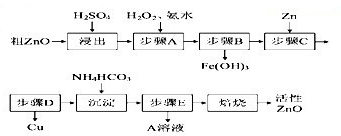
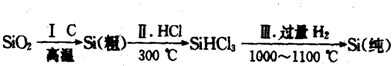��2012?������ģ��[��ѧ--ѡ��2����ѧ�뼼��]���Ṥҵ����Ӧ�����ۺϾ���Ч�����⣮
��1�����������ĸ�������ѡ��һ���½�һ�����᳧������Ϊ��ַ��ѡ��
C
C
�Ľ�����
A����������������
B��������������Ĺ�ҵ����
C���˿ڳ��ܵ��Ļ�����ҵ���ij���
��2��д������¯�����ջ�����Ļ�ѧ����ʽ��
��
д���Ӵ����еĻ�ѧ����ʽ��
��
��3��CuFeS
2�ǻ�ͭ�����Ҫ�ɷ֣�����ʱCuFeS
2ת��ΪCuO��Fe
2O
3��SO
2���÷�Ӧ�Ļ�ѧ����ʽΪ
4CuFeS
2+13O
2 4CuO+2Fe
2O
3+8SO
24CuFeS
2+13O
2 4CuO+2Fe
2O
3+8SO
2��
��4�������Ṥҵ�Ʒ��У���������������˵��������������Ҫԭ����߶�����ȷ����
D
D
��
A������������ǰ��Ҫ���飬��Ϊ���Ļ��������ڿ����з�Ӧ
B���ӷ���¯������¯���辻������Ϊ¯���ж�������������ʷ�Ӧ
C��������������Ϊ��������ʱ��ʹ�ô���������������߶��������ת����
D������������98.3%��Ũ�������գ�Ŀ���Ƿ�ֹ�γ�������������������������Ч��
��5���±���ѹǿ��SO
2ƽ��ת���ʵ�Ӱ�죺
ѹǿMpa
ת����%
�¶�/�� |
0.1 |
0.5 |
1 |
10 |
| 400 |
99.2 |
99.6 |
99.7 |
99.9 |
����SO
2ת��ΪSO
3�ķ�Ӧ������ѹǿ��ʹת����
����
����
������ʵ�ʹ�ҵ�����г����ó�ѹ������������
��ѹ��SO2��ת�����Ѻܴ�
��ѹ��SO2��ת�����Ѻܴ�
��
��6�������᳧����¯�ų��Ŀ����к���Fe
2O
3��CuO��CuSO
4����CuO��SO
3�ڷ���¯�л��϶��ɣ�����������ͭ���������������¯�¶Ȳ�ͬ���仯���±���
| ����¯�¶� |
600 |
620 |
640 |
660 |
| ¯����CuSO4��������/% |
9.3 |
9.2 |
9.0 |
8.4 |
��֪CuSO
4�ڵ���660��ʱ����ֽ⣬���Ҫ�����ϱ���CuSO
4�������������¶����߶����͵�ԭ��
SO2ת��ΪSO3������Ӧ���ȵĿ��淴Ӧ���¶����ߣ�ƽ�����ƣ�SO3���ʵ������٣�����CuSO4�������٣����¶����ߣ�SO3���ʵ������٣���CuSO4�������٣�
SO2ת��ΪSO3������Ӧ���ȵĿ��淴Ӧ���¶����ߣ�ƽ�����ƣ�SO3���ʵ������٣�����CuSO4�������٣����¶����ߣ�SO3���ʵ������٣���CuSO4�������٣�
��

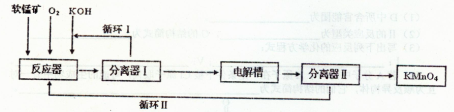


 ��1����Ԫ�¿�������ĩϵ�д�
��1����Ԫ�¿�������ĩϵ�д�