
����Ŀ������������л�������֮һ���Dz��鶯���ijЩ�������ڵ����ʴ�л�ֽ����Ҫ�����ղ��
(1)����[(NH2)2CO]�Ǻ�������ߵĹ��嵪�ʣ������ۺ�����Ϊ________%������ 1 λС������������ N �Ļ��ϼ�Ϊ________.
(2)������̼�����ڸ��¡���ѹ�ºϳɰ�������泥�����������ٷ����ֽⷴӦ�ɵõ����ء�д���÷ֽⷴӦ�Ļ�ѧ����ʽ��____________________________��
(3)��������(NH2)2CO ˮ��Һ���յ������� NOx�����չ����д��� HNO2 ��(NH2)2CO ���� N2 ��CO2 �ķ�Ӧ��д���÷�Ӧ�Ļ�ѧ����ʽ_______________________________ ������ 1 mol N2 ʱ��ת�Ƶĵ�����Ϊ __________ .
(4)Ҳ����ˮ���յ������� NOx����֪ NO2 ����ˮ������Ȼ�ѧ����ʽ���£�
2NO2��g��+H2O��l��![]() HNO3��aq��+HNO2��aq�� ��H=116.1 kJ��mol1
HNO3��aq��+HNO2��aq�� ��H=116.1 kJ��mol1
3NO2��g��+H2O��l��![]() 2HNO3��aq��+NO��g�� ��H=136.2kJ��mol1��
2HNO3��aq��+NO��g�� ��H=136.2kJ��mol1��
����ϡ��������NO�ķ�ӦHNO3��aq��+2NO��g��+H2O��l��=3HNO2��aq����H=___kJ��mol1
���𰸡�46.7% ��3 NH2-COONH4 = (NH2)2CO+H2O 2HNO2+(NH2)2CO = 2N2��+ CO2��+3H2O 3NA 75.9
��������
(1)����[(NH2)2CO]�����ۺ��������������е�Ԫ�ص��������������ؽṹʽΪ![]() ����ͼ��֪��ÿ��Nԭ���γ��������Թ��ۼ���N�ķǽ�����ǿ��C��H�����Ӷ�ƫ��ԭ�ӣ�NΪ-3�ۡ�
����ͼ��֪��ÿ��Nԭ���γ��������Թ��ۼ���N�ķǽ�����ǿ��C��H�����Ӷ�ƫ��ԭ�ӣ�NΪ-3�ۡ�
(2) ���л���������������ŵĽṹ��д����������淋Ļ�ѧʽΪ�� H2N-COONH4���ٸ��������������أ����������غ㶨��д����Ӧ����ʽ��
(3)��Ӧ��Ϊ HNO2 ��(NH2)2CO ���������� N2 ��CO2 �����������غ�͵�ʧ�����غ���д����ʽ�����ݵ���ת����Ŀ���㵱���� 1 mol N2 ʱ��ת�Ƶĵ�������
(4)�ɸ�˹���ɵó�Ŀ�귴Ӧ���ʱ䡣
(1)CO(NH2)2 �е�Ԫ�صİٷֺ���Ϊ�� 2��14/(12+16+28+4)=0.467 ���������ϵ���ֵ,һ������ 46.7%��, ��Ϊ�������ʣ����صĽṹ��ʽΪ H2N-CO-NH2,�ɻ��ϼ۹���֪̼�뵪��ʱ��Ϊ���ۣ�����̼��ʱ��Ϊ���ۣ���������ʱ��Ϊ���ۣ�CO(NH2)2 �� C �ǣ�4 �ۣ�O �ǣ�2�ۣ�H �ǣ�1 �ۣ�N ��-3 �ۡ���Ϊ��46.7% ����3��
(2)���л���������������ŵĽṹ֪������������� H2N-COONH4���������غ�֪�����ֽⷴӦ�õ����غ�ˮ H2N-COONH4 = (NH2)2CO+H2O ����Ϊ��NH2-COONH4 = (NH2)2CO+H2O��
(3) ��ȷ��Ԫ�صĻ��ϼ��ǽ�����С���ǰ�ᣬ�ɵ�ʧ�����غ��������غ����ƽ��Ӧʽ 2HNO2+(NH2)2CO = 2N2+ CO2 +3H2O�����ó����� 1 mol N2 ʱ��ת�Ƶĵ���Ϊ 3mol����Ϊ��2HNO2+(NH2)2CO = 2N2��+ CO2��+3H2O��3NA ��
(4)�ɸ�˹����֪������֪�� 3����Ӧ1��ȥ2����Ӧ2 ���ɵ�Ŀ�귴Ӧ ���ʡ� H=3����116.1 kJ��mol1) 2��(136.2kJ��mol1) =75.9 kJ��mol1����Ϊ��75.9��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��̬����C 85.7%����H 14.3%���ڱ�״���µ��ܶ���2.5g/L����������ײⶨ���������к�һ��˫����
��1���������ʵ��ʽ��
��2��������ķ���ʽ��
��3����д�����ĸ���ͬ���칹��Ľṹ��ʽ�����ƣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�������Ƹ����������ȵ� 600����Էֽ⣬ʵ����������ͼ�����������Ǵ������
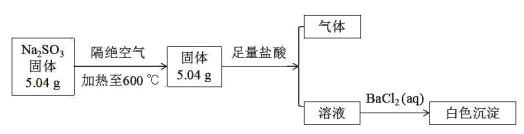
(1)��Ԫ����Ԫ�����ڱ��е�λ��_________________���������к��еĻ�ѧ������ _________________ .
(2)д�������������ȷֽ�Ļ�ѧ����ʽ _________________ .
(3)����˵����ȷ���� _________________ .
A�����ȷֽ��Ĺ�������Ԫ������Ϊ 1.92 ��
B�����ɰ�ɫ���������ʵ��� 0.04mol
C���ֽ���������ˮ����Һ������Ũ�ȴ�С˳��Ϊc(Na+)> c(SO42-)>c(S2-)>c(OH-)>c(HS-)>c(H+)
D������������������ֽ��Ĺ����ϣ��ټ�ϡ������ܻ���ֳ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. ij�־��нϺ������ԡ���ˮ�Ժ�Ƶ���Ե�Եĸ߷��ӻ�����ĽṹƬ������ͼ������֬����3�ֵ���ͨ�����۷�Ӧ�Ʊ�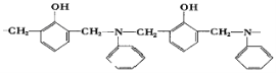
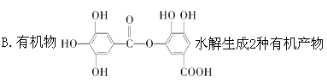
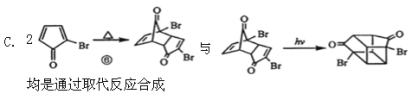
D.��֪ ![]() ���ϳ�
���ϳ�![]() ���õ���ʼԭ��ֻ����2��1,3����ϩ��2��Ȳ
���õ���ʼԭ��ֻ����2��1,3����ϩ��2��Ȳ
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��X��Y��Z��M��N��A ��Ϊ��ѧ��ѧ�еij������ʡ������������P������ȥ��
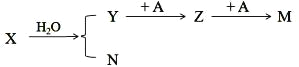
(1)�� X Ϊ����ɫ���壬A Ϊ�ճ�������Ӧ����㷺�Ľ�����д�� X �� H2O ��Ӧ�Ļ�ѧ����ʽ: __��Z Ϊ_________��д��ѧʽ����
(2)�� X Ϊ����ɫ���壬M Ϊ������ˮ�����ʣ��� X �� M ������ͬ��Ħ���������� X �ĵ���ʽ _______��A �вμӷ�Ӧ�������ӵĽṹʾ��ͼΪ_________________ ���� 1mol X ��ˮ��Ӧ������ת�����ܵõ� M ���������__
(3)�� M��N Ϊͬһ���ʣ���Ϊ������ij���õ�ζƷ��Ҫ�ɷ֡�д�� Y �� N ��Ӧ���� X �ķ�Ӧ���ͣ�_____������ Y ���Ƿ���� M �ļ��ʵ�鷽��___________________________________ .��ʢ���� KMnO4 ��Һ���Թ����ȵ����������ᣬ�ٵμ� Y�������ɫ��ȥ�������� M��д��������Ӧ�����ӷ���ʽ__________________________________.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ķ���ʽΪC18H17ClO2 ���䷢��ת����Ӧ�Ĺ�������ͼ��
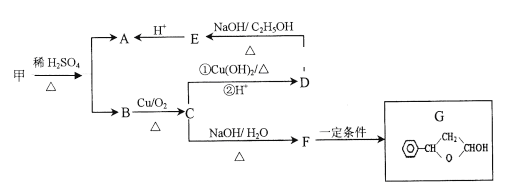
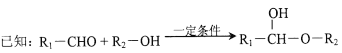
�ش��������⣺
��1��A�Ļ�ѧ����Ϊ_______________��A�����������____��ԭ�Ӵ���ͬһƽ���ϡ�
��2��C��F�ķ�Ӧ����Ϊ____________��F�к�������������Ϊ_____________________��
��3���������Ӧ����A��B�Ļ�ѧ����ʽΪ________________________��
��4��A�ж���ͬ���칹�壬д��2�ַ���������ͬ���칹��Ľṹ��ʽ
�������巢���ӳɷ�Ӧ
�ڷ����к�����������NaOH��Һ�з���ˮ�ⷴӦ
�ۺ˴Ź���������5��壬�������Ϊ1��2��2��1��2����_____________________��
��5��![]() ����Ҫ���л��ϳɹ�ҵ�м���֮һ���㷺����ҽҩ�����ϡ����Ϻй���֬�Ȼ�����Ʒ������������Ӧ·�ߣ����һ����AΪԭ�Ϻϳɵ�
����Ҫ���л��ϳɹ�ҵ�м���֮һ���㷺����ҽҩ�����ϡ����Ϻй���֬�Ȼ�����Ʒ������������Ӧ·�ߣ����һ����AΪԭ�Ϻϳɵ�![]() ·��(�����Լ���ѡ)__________________________________��
·��(�����Լ���ѡ)__________________________________��
��6�������칹����һ����ʽΪ˳���칹������ͬԭ�ӻ������˫��ƽ��ͬһ��ʱΪ˳ʽ�ṹ�������ʱΪ��ʽ�ṹ����![]() �ľۺ���˳ʽ�ṹ��ʽΪ__________��
�ľۺ���˳ʽ�ṹ��ʽΪ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��A�з�������ϸͭ˿������ձ��з�����ˮ���Թ�B�з����Ҵ����ұ��Թ�C�з�����ˮ����B�в��Ϲ��������ʹ�Ҵ������Ϳ���ͨ�����������ȵ�ͭ˿��
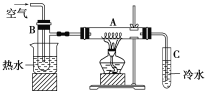
(1)A������Ϊ________����ˮ��������____________����ʵ���Ŀ����__________��
(2)�����Ҵ����Ƿ���ˮ�ķ���Ϊ_____________����ȥ����ˮ�ķ���Ϊ__________����ȥA���ƾ��ƺ�ͭ˿���ܱ��ֺ��ȵ�ԭ����____________________________��
(3)��Ӧ���Թ�C�е�Һ����ȴ��ȡ���������μӼ���������Һ����ˮԡ����һ��ʱ��۲쵽������Ϊ_________________����Ӧ����ʽΪ_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��˫����A�Ķ�����ϩ������һ����ʹ�˼�������ڷ���ϵͳ�������ң�������������ֳ�쳣�Ļ������أ���ṹ��ʽΪ��
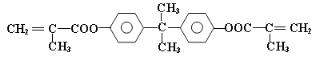
����һ��������ˮ�������˫����A������H�������ʡ�
I����1��˫����A�ķ���ʽΪ____________�������й�������������ȷ����________��
A���뱽�ӻ�Ϊͬϵ��
B�����Ժ�Na2CO3��Һ��Ӧ���ų�CO2����
C�������������13��̼ԭ����ͬһƽ����
D��1mol ˫����A����ˮ��Ӧ���������Br2�����ʵ���Ϊ4mol
��2��������������˫����A��Ϊͬ���칹�����_________������ţ���
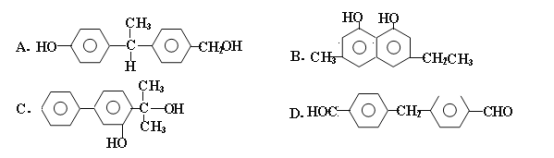
II����֪ȩ�ܱ�������Ϊ���ᡣ
![]()
����H����������;���Ƶã��еķ�Ӧ����û�б������
![]()
��3��C�Ľṹ��ʽΪ__________________��
��4��G������������Ϊ____________�������ƣ���G��H�ķ�Ӧ����Ϊ__________��
��5��E��F�Ļ�ѧ����ʽΪ____________________________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com