
由实验得知用电解法将电解液中的金属离子还原为金属单质时,电极所通过的电荷量Q正比于金属的物质的量n和金属离子化合价a的乘积,Q=F·na,其中F是一恒量,称为法拉第常数,它与金属的种类无关(阿伏加德罗常数NA=6.023×1023 mol-1,电子电荷量e=1.6×10-19 C,Cu的摩尔质量:64×10-3 kg·mol-1)。
(1)试求出法拉第常数F(电荷量以库仑为单位,保留三位有效数字)。
(2)如果电解硫酸铜溶液获得1 kg的金属铜,通过电解槽的电荷量是多少?
(3)用电镀的方法在半径为R的铜球表面均匀地镀上很薄的银层,在电镀槽中铜球是阳极还是阴极?另一电极是什么材料?若电流为I,通电时间为t,银的相对原子质量为A,金属银的密度为ρ,求镀层的厚度d。
(1)F=9.64×104 C·mol-1
(2)Q=3.0×106 C
(3)阴极;银;d=![]()
(1)由题意可知F=![]() ,其中na乘积为转移的电子的物质的量,所以法拉第常数F的含义是1 mol电子的电荷量,即F=NA×e,代入数据可得
,其中na乘积为转移的电子的物质的量,所以法拉第常数F的含义是1 mol电子的电荷量,即F=NA×e,代入数据可得
F=NA×e=1.60×10-19C×6.023×1023 mol-1=9.64×104 C·mol-1。
(2)1 kg 铜的物质的量n=![]() =15.6 mol,铜离子a=2,则电荷量Q=Fna=9.64×104 C·mol-1×15.6 mol×2=3.0×106 C。
=15.6 mol,铜离子a=2,则电荷量Q=Fna=9.64×104 C·mol-1×15.6 mol×2=3.0×106 C。
(3)由电解原理可知:待镀金属作阴极,镀层金属作阳极。确定铜球是阴极,阳极材料是银。由电解定律可得出通过的电荷量Q=Fna,其中a=1,析出银的物质的量n=![]() ;
;
则可推知厚度d=![]() 。
。


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源:物理教研室 题型:038
查看答案和解析>>
科目:高中化学 来源: 题型:038
由实验得知,用电解法将电解液中的金属离子还原为金属单质时,电极所通过的电量Q正比于金属的物质的量n和金属离子化合价a的乘积,其比例系数F是一个恒量,称为法拉第常数,它与金属的种类无关。阿伏加德罗常数:NA=6.02´1023mol-1,电子电量:e=1.60´10-19C,Cu的摩尔质量:64´10-3kg/mol。(1)试求出法拉第常数F(电量以库仑为单位,保留三位有效数字)。(2)如果电解硫酸铜溶液获得1kg的金属铜,通过电解槽的电量是多少?(3)用电镀的方法在半径为R的铜壳表面上均匀镀上很薄的银层,在电解槽中铜球是阳极还是阴极?另一电极是什么材料?(4)若电流强度为I,通电时间为t,银的相对原子质量为A,金属银的密度为r,求镀层的厚度d(用题中的符号表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)试求出法拉第常数F(电量以库仑为单位,保留三位有效数字)。
(2)如果电解硫酸铜溶液获得1 kg的金属铜,通过电解槽的电荷量是多少?
(3)用电镀的方法在半径为R的铜球表面均匀地镀上很薄的银层,在电镀槽中铜球是阳极还是阴极?另一电极是什么材料?若电流为I,通电时间为t,银的相对原子质量为A,金属银的密度为ρ,求镀层的厚度d。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
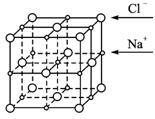
NaCl晶体结构示意图
图1-1-1
(1)将固体NaCl细粒干燥后,准确称取m g NaCl固体并转移到定容仪器A中;
(2)用滴定管向A仪器中加苯,不断振荡,继续加苯至A仪器的刻度,计算出NaCl固体的体积V cm3。
请回答下列问题:
①步骤(1)中A仪器最好使用__________ (填序号)。
A.量筒 B.烧杯 C.容量瓶 D.试管
②步骤(2)中用酸式滴定管还是用碱式滴定管__________,理由是____________________。
③能否用水代替苯__________,理由是___________________________________________。
④已知NaCl晶体中,靠得最近的Na+与Cl-间的平均距离为a cm(如图1-1-1),用上述测定方法测得的阿伏加德罗常数NA的表达式为_________________________________________。
(3)另一种方法是电解法,方法是:用铂电极电解CuCl2溶液时,当电流为I,通电时间为t(单位:分钟)时,阴极增加的质量为m,在阳极收集到气体体积(标准状况)为V。又知1个电子的电荷量为Q,铜的摩尔质量为M,则计算阿伏加德罗常数NA的算式为( )
A.It/QV B.32It/mQ C.672It/QV D.30MIt/mQ
(4)由实验得知,用电解法将电解液中的金属离子还原为金属单质时,电极所通过的电量Q正比于金属的物质的量n和金属离子的化合价a的乘积,其比例系数F是一恒量,称为法拉第常数。它与金属的种类无关。
用电镀法在半径为R的铜球表面均匀镀上很薄的银层,在电解槽中铜球作__________极,另一电极材料是__________。若电流为I,通电时间为t,银的相对原子质量为A,金属银的密度为ρ,求镀层的厚度d(用本题中的符号表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com