
“绿色化学”是当今社会提出的一个新概念。在“绿色化学”工艺中,理想状态是反应中原子全部转化为要制取的产物,即原子利用率为100%。以下反应最符合绿色化学原子经济性要求的是
A. 乙烯发生加聚反应制得聚乙烯高分子材料
B. 用甲烷与氯气制备一氯甲烷
C. 用石灰石和稀盐酸反应制得二氧化碳
D. 用苯和液溴为原料制取溴苯
科目:高中化学 来源:2015-2016学年江西省高二下期末化学试卷(解析版) 题型:实验题
某兴趣小组对NO与Na2O2的反应进行了探究。通过查阅资料可知:①NO不与碱反应;②亚硝酸盐除浅黄色的AgNO2难溶于水外,其它都易溶于水;③2NaNO3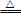 2NaNO2+O2↑,NaNO2热稳定性很高。
2NaNO2+O2↑,NaNO2热稳定性很高。
【实验探究Ⅰ】兴趣小组的同学经讨论设计了如下图所示实验:
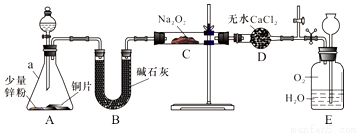
(1)装置B的作用是 ;
(2)在分液漏斗中加稀硝酸之前,先加入少量稀硫酸让A中锌粉完全溶解,其目的是 ;
(3)实验观察到C中固体颜色变白,E中气体先变红棕色,最终又变无色。E中总反应的化学方程式是 。
【实验探究Ⅱ】 该兴趣小组进一步探究C中生成的白色固体的成分。
(4)提出假设:
假设1. 白色固体只有NaNO3;
假设2. 白色固体只有_________________;
假设3. 白色固体是两种物质的混合物。
(5)实验验证:
①根据查阅的资料,要证明假设1是否成立,需要用到的试剂为____________________;
②为证明是假设2还是假设3成立,称取C中生成的白色固体m g置于坩埚中(坩埚质量为a g),用酒精灯加热至质量不再改变,若假设3成立,则冷却后称得剩余固体总质量n的范围是 。(用含字母的不等式表示)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年西藏日喀则一中高二6月月考化学试卷(解析版) 题型:选择题
下列变化过程属于物理变化的是
A.煤的燃烧 B.分馏石油 C.大米酿酒 D.金属的腐蚀
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一下期末化学试卷(解析版) 题型:选择题
一定温度下,在容积恒定的密闭容器中进行反应A(s)+2B(g)  C(g)+D(g),下列叙述能表明该反应已达到平衡状态的是
C(g)+D(g),下列叙述能表明该反应已达到平衡状态的是
①混合气体的密度不变
②容器内气体的压强不变
③混合气体的总物质的量不变
④B的物质的量浓度不变
⑤v正(C)=v逆(D)
⑥v正(B)=2v逆(C)
A.①④⑤⑥ B.②③⑥ C.②④⑤⑥ D.只有④
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一下期末化学试卷(解析版) 题型:选择题
以下实验能获得成功的是
A.用乙醇和乙酸混合共热制取乙酸乙酯
B.将铁屑、溴水、苯混合制溴苯
C.在苯中滴入浓硝酸制硝基苯
D.将铜丝在酒精灯加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏高二上学期期中化学试卷(解析版) 题型:填空题
已知A、B、C、D、E都是元素周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。B原子的p轨道半充满,形成的氢化物的沸点是同主族元素的氢化物中最低的。D原子得到一个电子后3p轨道全充满。A+比D原子形成的离子少一个电子层。C与A形成A2C型离子化合物。E的原子序数为26,E原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)

(1)A、B、C、D的第一电离能由小到大的顺序为____________________________。
(2)C的氢化物分子是 (填“极性”或“非极性”)分子。
(3)化合物BD3的分子空间构型是 。中心原子的杂化方式为 。
(4)金属E单质的晶体在不同温度下有两种堆积方式,晶胞如上图所示。体心立方晶胞和面心立方晶胞中实际含有的E原子个数之比为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏高二上学期期中化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A、1molNa2O2晶体中阴离子与阳离子之比为1:1
B、1molSi晶体中含4molSi—Si键
C、60gSiO2中含Si—O键的个数为4NA
D、12 g金刚石中含有C—C键的个数为NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高二下学期期末化学试卷(解析版) 题型:实验题
氢溴酸在医药和石化工业上有广泛用途。下图是模拟工业制备氢溴酸粗品并精制的流程。
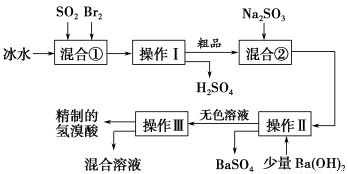
根据上述流程回答下列问题:
(1)混合①中发生反应的化学方程式为________________________________。
(2)混合①中使用冰水的目的是________________________________。
(3)操作Ⅱ和操作Ⅲ的名称分别是________、________。
(4)混合液②中加入Na2SO3的目的是_________________________________。
(5)纯净的氢溴酸应为无色液体,但实际工业生产中制得的氢溴酸(工业氢溴酸)常带有淡淡的黄色。于是甲、乙两同学设计了简单实验加以探究:甲同学假设工业氢溴酸呈淡黄色是因为含有Fe3+,则用于证明该假设所用的试剂为________,若假设成立可观察的现象为___________。乙同学假设工业氢溴酸呈淡黄色是因为________________________,其用于证明该假设所用的试剂为________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高二6月月考化学试卷(解析版) 题型:选择题
有镁、铝混合粉末10.2 g,将它溶于1000 mL,2 mol/L的盐酸中,若要使沉淀质量达到最大值,则需加入金属钠的质量为
A、46 g B、23 g C、4.6 g D、69 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com