
| A. | X的I1大于Y 的I1 | B. | X的电负性小于Y的电负性 | ||
| C. | X的阴离子半径小于Y的阳离子半径 | D. | X的原子半径大于Y的原子半径 |
分析 X的阴离子与Y的阳离子具有相同的电子层结构,X在Y的前一周期,可知原子半径、原子序数关系为Y>X,X为非金属,Y为金属,结合离子的性质解答该题.
解答 解:A.X为非金属元素不容易失去一个电子,Y为金属元素容易失去电子,所以X的第一电离能大于Y的第一电离能,故A正确;
B.X为非金属元素,Y为金属元素,所以X的电负性大于Y的电负性,故B错误;
C.X的阴离子与Y的阳离子具有相同的核外电子排布,核电荷数越大离子半径越小,故C错误;
D.X在Y的前一周期,则X的原子半径小于Y的原子半径,故D错误.
故选A.
点评 本题考查原子结构与元素周期律知识,题目难度中等,解答本题,根据原子结构的信息推断元素在周期表中的相对位置是解答该题的关键.


科目:高中化学 来源: 题型:选择题
| A. | 14C的原子结构示意图: | B. | 二氧化碳的电子式: | ||
| C. | H2O2的电子式: | D. | C3H8的结构式:CH3-CH2-CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | B | ||||||
| D | E | F | |||||
| C | I | G | H |
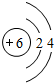 .
.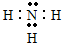 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
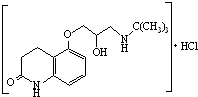 )可用于治疗心绞痛和青光眼.
)可用于治疗心绞痛和青光眼.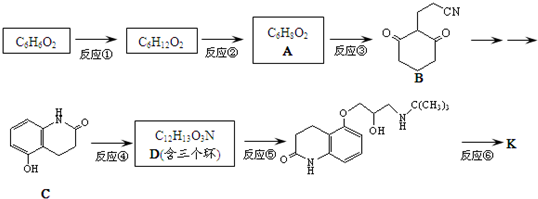
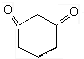 D
D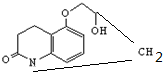
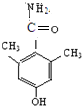 、
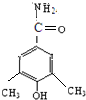
、
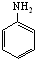 )与HNO2和H3PO2反应可得苯.请设计从C合成
)与HNO2和H3PO2反应可得苯.请设计从C合成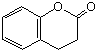 的路线.(合成路线常用的表示方法为:A$→_{反应条件}^{反应试剂}$B…$→_{反应条件}^{反应试剂}$目标产物)
的路线.(合成路线常用的表示方法为:A$→_{反应条件}^{反应试剂}$B…$→_{反应条件}^{反应试剂}$目标产物)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O:0.002 mol•L-1 | B. | NO:0.001 mol•L-1 | ||
| C. | NH3:0.002 mol•L-1 | D. | O2:0.0025 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 6.34 | 9.7 |
| Fe3+ | 1.48 | 3.2 |
| Zn2+ | 6.2 | 8.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

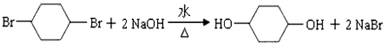 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属性:Na>Mg>Al | B. | 热稳定性:HCl>H2S>PH3 | ||
| C. | 碱性性强弱:NaOH>Mg(OH)2>Al(OH)3 | D. | 非金属性:F>Cl>S>O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com