
| A. | X、Y间可形成离子化合物 | |
| B. | 单质熔点:Y>W>X | |
| C. | 最高价氧化物对应水化物的酸性:Z>W | |
| D. | Y、W形成的单核离子均能破坏水的电离平衡 |
分析 短周期主族元素X、Y、Z、W原子序数依次增大,X-与氦原子电子层结构相同,则X为H元素;Y原子核外L层电子数为8且Y与X同主族,则Y为Na;Z原子的最外层电子数是内层电子总数的一半,Z为Si;W的最高正价与最低负价的代数和为4,最高价为+6价,最低价为-2价,则W为S元素,然后结合元素周期律及元素化合物知识来解答.
解答 解:短周期主族元素X、Y、Z、W原子序数依次增大,X-与氦原子电子层结构相同,则X为H元素;Y原子核外L层电子数为8且Y与X同主族,则Y为Na;Z原子的最外层电子数是内层电子总数的一半,Z为Si;W的最高正价与最低负价的代数和为4,最高价为+6价,最低价为-2价,则W为S元素,
A.X、Y间可形成离子化合物为NaH,故A正确;
B.一般熔点为金属晶体大于分子晶体,但Na的熔点较低,则单质熔点:W(110℃)>Y(97℃)>X,故B错误;
C.非金属性越强,对应最高价含氧酸的酸性越强,则最高价氧化物对应水化物的酸性:W>Z,故C错误;
D.Y形成的单核离子对水的电离平衡无影响,W形成的单核离子可促进水的电离平衡,故D错误;
故选A.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子结构、元素性质推断元素为解答的关键,侧重分析与推断能力的考查,注意周期律及元素化合物知识的应用,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径A>B>D>C | B. | 原子序数a>b>c>d | ||
| C. | 离子半径D>C>B>A | D. | 金属性B>A,非金属性D>C |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间/s | 0 | 2 | 4 | 6 | 8 | 10 |
| c(NO)/mol•L-1 | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol•L-1 | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
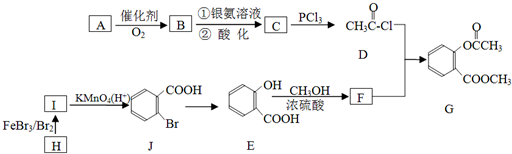
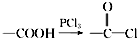 ,请回答以下问题:
,请回答以下问题: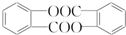 .
.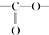 结构
结构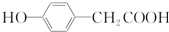 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
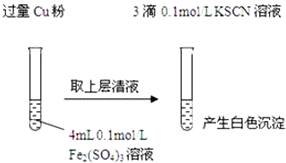
| 实验方案 | 现象 | 结论 |
| 步骤1:取4mL0.1mol/L CuSO4溶液,向其中滴加3滴0.1mol/L KSCN溶液 | 产生白色沉淀 | CuSO4与KSCN反应产生了白色沉淀 |
| 步骤2:取取4mL0.1mol/LFeSO4溶液,向其中滴加3滴0.1mol/LKSCN溶液 | 无明显现象 |
| 实验方案 | 现象 |
| 向3mL 0.1mol/L FeSO4溶液中加入1mL 8mol/L稀硝酸 | 溶液变为棕色,放置一段时间后,棕色消失,溶液变为黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com