
分析 乙烯与溴发生加成反应生成1,2-二溴乙烷,溴水增重1.4克为乙烯的质量,根据n=$\frac{V}{{V}_{m}}$计算混合气体总物质的量,根据n=$\frac{m}{M}$计算乙烯的物质的量,再计算乙烷的物质的量,根据V=nVm计算乙烷、乙烯的体积.
解答 解:(1)乙烯与溴发生加成反应,反应方程式为:CH2=CH2+Br2→BrCH2CH2Br,
答:乙烯与溴发生反应方程式为CH2=CH2+Br2→BrCH2CH2Br.
(2)溴水增重1.4克为乙烯的质量,则n(C2H4)=$\frac{1.4g}{28g/mol}$=0.05mol,
又n(C2H4)+n(C2H6)=$\frac{4.48L}{22.4L/mol}$=0.2mol,
则n(C2H6)=0.2mol-0.05mol=0.15mol,
故V(C2H4)=0.05mol×22.4l/mol=1.12L,
V(C2H6)=0.15mol×22.4l/mol=3.36L,
答:乙烯体积为1.12L,乙烷体积为3.36L.
点评 本题考查化混合物计算、乙烷和乙烯性质,试题贴近教材,基础性强,关键是明确乙烷和乙烯的性质差异.


科目:高中化学 来源: 题型:选择题
| A. | 8gCH4所含原子数目为2NA | |
| B. | 0.5mol H2O含有的氢原子数目为1.5NA | |
| C. | 常温常压下,48g O3含有的氧原子为3NA | |
| D. | 1L 1mol•L-1 Na2SO4溶液中含有的氧原子为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C、D是元素周期表中前36号元素,它们的核电荷数依次增大.第二周期元素A原子的核外成对电子数是未成对电子数的2倍且有3个能级,B原子的最外层p轨道的电子为半充满结构,C是地壳中含量最多的元素.D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满.请回答下列问题:
A、B、C、D是元素周期表中前36号元素,它们的核电荷数依次增大.第二周期元素A原子的核外成对电子数是未成对电子数的2倍且有3个能级,B原子的最外层p轨道的电子为半充满结构,C是地壳中含量最多的元素.D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | K+ Na+ Cu2+ Al3+ |
| 阴离子 | SO42- HCO3-OH- Cl- |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{92}^{235}$U相对原子质量为235 | |
| B. | ${\;}_{92}^{235}$U中的中子数为92 | |
| C. | ${\;}_{92}^{235}$U与 ${\;}_{6}^{12}$C的质量比约为235:12 | |
| D. | ${\;}_{92}^{235}$U 与${\;}_{92}^{238}$U互称为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 元素 | 相关信息 |
| X | X元素可形成自然界中硬度最大的物质 |
| Y | 其单质为双原子分子,其最简单氢化物的水溶液能使酚酞变红 |
| Z | Z是短周期内最容易失去电子的元素 |
| M | M的一种同位素的质量数为34,中子数为18 |
| N | N是具有紫红色光泽的金属,有很好的延展性、导热性和导电性 |
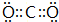 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com