
【题目】对乙酰氨基苯酚M( ![]() )是最常见的消炎解热镇痛药,用于治疗感冒发烧和关节痛等.M的一种合成路线如下:
)是最常见的消炎解热镇痛药,用于治疗感冒发烧和关节痛等.M的一种合成路线如下: 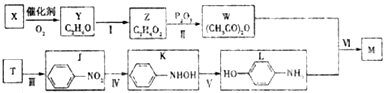
已知:①X,Y,T分子的核碰共振氢谱只显示1组峰,且X能使溴水褪色;
② ![]() .
.
(1)X,Y的结构简式为、;
(2)Ⅲ的反应类型为 , Ⅵ的反应方程式为;
(3)M与足量氢氧化钠溶液反应的化学方程式为;
(4)M有多种同分异构体,其中一类与J互为同系物且氮原子与苯环直接相连,此类同分异构体共有种; 另一类同分异构体同时满足下列条件①属于对位二取代苯且苯环上连有﹣NH2;②能发生水解反应;③核碰共振氢谱有4组峰.写出其中一种同分异构体的结构简式 .
【答案】
(1)CH2=CH2;![]()
(2)取代反应;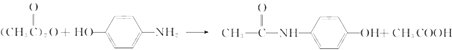
(3)![]()
(4)9;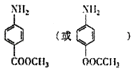
【解析】解:根据流程图知,X中含有两个C原子,X发生氧化反应生成Y;X,Y,T分子的核碰共振氢谱只显示1组峰,且X能使溴水褪色,则X为CH2=CH2 , X被催化氧化得到Y,根据Y分子式及核磁共振氢谱知,Y结构简式为 ![]() ;Y发生反应生成Z,根据Z分子式、W结构简式知,反应I为加成反应,Z结构简式为CH3COOH,反应II为取代反应,W结构简式为CH3COOOCCH3; T分子的核碰共振氢谱只显示1组峰,根据J结构简式知,T发生取代反应生成J,则T结构简式为
;Y发生反应生成Z,根据Z分子式、W结构简式知,反应I为加成反应,Z结构简式为CH3COOH,反应II为取代反应,W结构简式为CH3COOOCCH3; T分子的核碰共振氢谱只显示1组峰,根据J结构简式知,T发生取代反应生成J,则T结构简式为 ![]() ,结合各物质结构简式知,IV为取代反应,W和L发生取代反应生成M,(1)通过以上分析知,X、Y结构简式分别为CH2=CH2、
,结合各物质结构简式知,IV为取代反应,W和L发生取代反应生成M,(1)通过以上分析知,X、Y结构简式分别为CH2=CH2、 ![]() ,所以答案是:CH2=CH2;
,所以答案是:CH2=CH2; ![]() ;(2)通过以上分析知,III为取代反应,VI的方程式为
;(2)通过以上分析知,III为取代反应,VI的方程式为 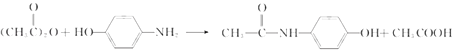 ,所以答案是:取代反应;
,所以答案是:取代反应; 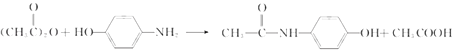 ;(3)M中肽键水解生成的羧基及M中酚羟基都能与NaOH反应,反应方程式为
;(3)M中肽键水解生成的羧基及M中酚羟基都能与NaOH反应,反应方程式为 ![]() ,所以答案是:
,所以答案是: ![]() ;(4)M为
;(4)M为 ![]() ,M有多种同分异构体,其中一类与J互为同系物,说明含有苯环和硝基,且氮原子与苯环直接相连,如果存在﹣CH2COOH基团,有邻间对三种结构;如果存在HCOOCH2﹣基团,有邻间对三种结构,如果存在CH3CONH﹣、﹣OH基团,有邻间对三种结构,所以符合条件的有9种;另一类同分异构体同时满足下列条件①属于对位二取代苯且苯环上连有﹣NH2;②能发生水解反应说明含有酯基;③核碰共振氢谱有4组峰,说明含有4种氢原子,符合条件的结构简式为
,M有多种同分异构体,其中一类与J互为同系物,说明含有苯环和硝基,且氮原子与苯环直接相连,如果存在﹣CH2COOH基团,有邻间对三种结构;如果存在HCOOCH2﹣基团,有邻间对三种结构,如果存在CH3CONH﹣、﹣OH基团,有邻间对三种结构,所以符合条件的有9种;另一类同分异构体同时满足下列条件①属于对位二取代苯且苯环上连有﹣NH2;②能发生水解反应说明含有酯基;③核碰共振氢谱有4组峰,说明含有4种氢原子,符合条件的结构简式为 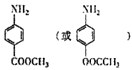 ,所以答案是:9种
,所以答案是:9种  ;
;


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
【题目】下列各组离子中因有配离子生成而不能大量共存的是( )
A. K+、Na+、Cl-、NO3-B. Mg2+、Ca2+、SO42-、OH-
C. Fe2+、Fe3+、H+、NO3-D. Ba2+、Fe3+、Cl-、SCN-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组同学用如图装置进行实验,下列有关说法中,正确的是( ) 
A.若X、Y、Z分别为铁片、铜片、氯化铜溶液,开关K与a连接,则Y极上有气泡放出
B.若X、Y、Z分别为铁片、铜片、氯化铜溶液,开关K与a连接,则溶液中Cu2+向Y极移动
C.若X、Y、Z分别为石墨、石墨、氯化铜溶液,开关K与b连接,则溶液中Cu2+向Y极移动
D.若X、Y、Z分别为石墨、石墨、氯化铜溶液,开关K与b连接,则 Y极上有黄绿色气体生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于实验内容与结论相符合的是( )
实验内容 | 结论 | |
A | 向某溶液中滴加BaCl2溶液,产生白色沉淀 | 溶液中有SO |
B | 向某溶液中滴加AgNO3溶液,产生白色沉淀 | 溶液中有Cl﹣ |
C | 向某溶液中滴加少量KSCN溶液,溶液变红 | 溶液中有Fe3+ |
D | 向某溶液中滴加一定量的NaOH溶液,生成白色沉淀 | 溶液中有Al3+ |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤炭可以转化为清洁能源和化工原料.
(1)用煤可以制得水煤气.工业上可用煤和水通过水煤气法制氢气,已知下列热化学方程式:
C(s)+ ![]() O2(g)═CO(g)△H1=﹣110.5kJmol﹣1
O2(g)═CO(g)△H1=﹣110.5kJmol﹣1
2H2(g)+O2(g)═2H2O(g)△H2=﹣483.6kJmol﹣1
试求水煤气法制氢气的反应的反应热△H3 .
C(s)+H2O(g)═CO(g)+H2(g)△H3=kJmol﹣1
(2)若H﹣H、O=O和O﹣H键的键能分别是436kJmol﹣1、496kJmol﹣1和m kJmol﹣1 , 结合上述热化学方程式的相关数据计算,m= .
(3)已知一氧化碳与水蒸气反应过程的能量变化如图所示:则此反应为(填“吸热”或“放热”)反应,反应的热化学方程式为 . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将AlCl3溶液和NaAlO2溶液分别蒸发并灼烧,所得产物的主要成份是( )
A.均为Al(OH)3
B.前者得Al2O3,后者得NaAlO2
C.均为Al2O3
D.前者得AlCl3,后者得NaAlO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,取20mL某浓度的盐酸作为待测液,用一定物质的量浓度的NaOH溶液进行滴定(假设盐酸与NaOH溶液混合后体积变化忽略不计),滴定过程中溶液的pH变化如右图所示。下列叙述正确的是( ) 
A.所用盐酸的浓度是0.09mol·L─1 , NaOH溶液浓度为0.03mol·L─1
B.在B点,溶液中离子浓度关系为:c(Cl─)>c(Na+)>c(OH-)>c(H+)
C.A,B,C三点水的电离程度大小依次为:A>B>C
D.滴定前,锥形瓶用待测液润洗,导致盐酸浓度偏低
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com