
| �� | �� | �ƼغϽ�������1��3�� | |
| �۵�/�� | 97.9 | 63.5 | ��-10 |
���� ��1���Ͻ��Ӳ�ȱ��䴿����С���۵���䴿�����ͣ�
��2�����ƺϽ�������õĵ����ԣ��۵�ͣ���Ϊ��ȴ����
��3�����ƺϽ���ԺͿ����ijɷ�֮�䷴Ӧ�����Ǻ��������Ӧ��
��4�����ƺϽ���ˮ�����ҷ�Ӧ���ɼ��������
��� �⣺��1���Ͻ���ص㣺Ӳ�ȱ��䴿����С���۵���䴿�����ͣ��ʴ�Ϊ��С���ͣ�
��2�����ƺϽ�������õĵ����ԣ��۵�ͣ���Ϊ��ȴ�����ʴ�Ϊ�������ԣ�
��3���Ʊ����ƺϽ�������������ォ�����ֹ���ҡ�Σ��������ڻ�������䵱�����������Ը�����������ֹ�����ƺͽ����غͿ����ɷַ�Ӧ���ʴ�Ϊ��������������ֹ�����ƺͽ����غͿ����ɷַ�Ӧ��
��4�����ƺϽ���ˮ�����ҷ�Ӧ���ɼ����������2Na+2H2O=2NaOH+H2����2K+2H2O=2KOH+H2�����ʴ�Ϊ��2Na+2H2O=2NaOH+H2����2K+2H2O=2KOH+H2����
���� ���⿼��ѧ�������ƺͽ����ص������Լ��Ͻ���ص�֪ʶ��ע��֪ʶ�����Ӧ���ǹؼ����Ѷ��еȣ�


 ͨ��ѧ��Ĭд����ϵ�д�
ͨ��ѧ��Ĭд����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ڢ� | C�� | �٢� | D�� | �ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  Al2��SO4��2 | B�� |  KAl��SO4��2 | C�� |  NH4Al��SO4��2 | D�� |  NH4Al��SO4��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �٢ۢ� | C�� | �٢� | D�� | �ڢۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
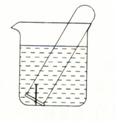 ͼ��ʾˮ���е��Թ�����һö��������������̿�������������۲죺
ͼ��ʾˮ���е��Թ�����һö��������������̿�������������۲죺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
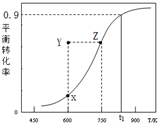 �״��������ȡ��ȩCH3OH��g��?HCHO��g��+H2��g�����״���ƽ��ת�������¶ȱ仯������ͼ��ʾ�������й�˵����ȷ���ǣ�������
�״��������ȡ��ȩCH3OH��g��?HCHO��g��+H2��g�����״���ƽ��ת�������¶ȱ仯������ͼ��ʾ�������й�˵����ȷ���ǣ�������| A�� | ���ⷴӦ�ġ�H��0 | B�� | ��t1Kʱ���÷�Ӧ��ƽ�ⳣ��Ϊ8.1 | ||
| C�� | 600Kʱ��Y��״��Ħԣ��������ԣ��棩 | D�� | ��������ϵѹǿ�����߽�����ƽ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
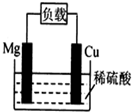
| A�� | ��ط�ӦΪ��Mg+2H+=Mg2++H2�� | B�� | þ��������ԭ��Ӧ | ||
| C�� | ���Ӵ�ͭ�������·����þ�� | D�� | ͭ��Ϊ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HCO3-һ�����ܴ��������ڸ���Һ�� | |
| B�� | NH4+һ�����ܴ��������ڸ���Һ�� | |
| C�� | ����Һ��pHһ��Ϊ12 | |
| D�� | ����Һ��c��H+��=c��OH-�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com