
 ��H2��O2��������Na2CO3���ȼ�ϵ�أ����õ�ⷨ�Ʊ�Fe��OH��2��װ����ͼ��ʾ������P��ͨ��CO2��
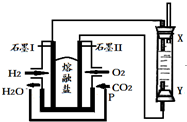
��H2��O2��������Na2CO3���ȼ�ϵ�أ����õ�ⷨ�Ʊ�Fe��OH��2��װ����ͼ��ʾ������P��ͨ��CO2������ ������װ��ͼ������ʯī�缫����ͨ������������������Ӧ������ʧȥ������������Na2CO3���ȼ�ϵ���з�Ӧ����ˮ��Ϊ�������Դ˽��
������װ��ͼ������ʯī�缫����ͨ������������������Ӧ������ʧȥ������������Na2CO3���ȼ�ϵ���з�Ӧ����ˮ��Ϊ������ͨ��������һ��Ϊ���������ʱ��XΪ������YΪ��������������ʧ���������������ӣ�X�缫�����ӵõ�������������������������Ũ������������������������������������Դ˽��
��� �⣺������װ��ͼ������ʯī�缫����ͨ������������������Ӧ������ʧȥ������������Na2CO3���ȼ�ϵ���з�Ӧ����ˮ������H2-2e-+CO32-=CO2+H2O���ʴ�Ϊ��H2-2e-+CO32-=CO2+H2O��
��A��X��Y���ˣ�����Y���������缫��X�缫����Ҫһ���������缫��������ʯī�缫����A����
B���������������������ӷŵ�õ���Һ�е����������ӽ������������������������������Կ�����NaOH��Һ��Ϊ���Һ����B��ȷ��
C�����������ķ�Ӧ����Һ�е������ӵõ�������������������Һ�е缫��Ӧ��2H2O+2e-=H2��+2OH-����C��ȷ��
D����ɫ����ֻ���������ϲ�����������̷���������������������Ҳ��������������������������������D����
��ѡBC��
���� ���⿼�����͵�أ�Ϊ��Ƶ���㣬��Ŀ�ѶȲ���ע�����ԭ��صĹ���ԭ���Լ��缫��Ӧʽ����д�������Ĺؼ��Ǹ������ʵ������ж�ԭ��ص���������


 ������������Ӧ����ϵ�д�
������������Ӧ����ϵ�д� ͬ����չ�Ķ�ϵ�д�
ͬ����չ�Ķ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ˮ������֮Դ���������ǵ�����������أ��ڻ�ѧʵ��Ϳ�ѧ�о��У�ˮҲ��һ�ֳ��õ��Լ���
ˮ������֮Դ���������ǵ�����������أ��ڻ�ѧʵ��Ϳ�ѧ�о��У�ˮҲ��һ�ֳ��õ��Լ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
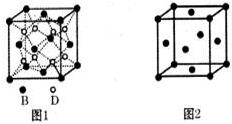
 ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ʵ����� | ���� | ���� |
| A | ��KI��FeCl3��Һ���Թ��л�Ϻ���CCl4������ | �²���Ϻ�ɫ | �����ԣ�Fe3+��I2 |
| B | ��ϡ�����м����������� | ��Һ��Ϊ��ɫ | ϡ���ὫFe������Fe3+ |
| C | ��ʢNa2SiO3 ��Һ���Թ��еμ�1�η�̪��Һ��Ȼ����μ���ϡ��������ɫ�ӽ���ʧʱֹͣ������ | �Թ���������� | �ǽ����ԣ�Cl��Si |
| D | ��������Һ�����Ƶ�������ͭ��ϼ��� | ��ש��ɫ�������� | �����Ƿ��������ǻ� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ӽ� | B�� | ���Լ� | C�� | �Ǽ��Լ� | D�� | ���»��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ����������Ƶ����������Ӱ�����ҹ��������������о���ʾ������Ҫ��Ⱦ��Ϊ�����������PM2.5��ȼú�����������ﳾ�������Ⱦ����Ҫԭ����ˣ����û�ѧ�����δ�����Ⱦ�ǵ�����Ҫ���о�����
����������Ƶ����������Ӱ�����ҹ��������������о���ʾ������Ҫ��Ⱦ��Ϊ�����������PM2.5��ȼú�����������ﳾ�������Ⱦ����Ҫԭ����ˣ����û�ѧ�����δ�����Ⱦ�ǵ�����Ҫ���о�����| ���� | Na+ | K+ | NH4+ | NO3- | SO42- | Cl- |
| Ũ��/mol•L-1 | 7��10-6 | 3��10-6 | 2��10-5 | 5��10-5 | 3��10-5 | 2��10-5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ�Ӿ�����һ����������Ԫ�� | |
| B�� | ���Ӿ�����һ���������� | |
| C�� | ��������һ����������������Ϊ2��8 | |
| D�� | H2O��һ�ַdz��ȶ��Ļ������������������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com