
从食品店购买的蔗糖配成溶液,做银镜反应实验,往往能得到银镜。产生这一现象的原因是( )
A.蔗糖本身有还原性
B.蔗糖被还原
C.实验过程中蔗糖发生水解
D.在生产和贮存过程中蔗糖有部分水解
科目:高中化学 来源: 题型:
A、B两种有机物的最简式均为CH2O,下列关于它们的叙述中,正确的是( )
A.它们互为同系物
B.它们互为同分异构体
C.它们燃烧后产生的CO2和H2O物质的量之比为1:1
D.取等物质的量的A、B,完全燃烧后所消耗的O2的物质的量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为CH3CH2OH-4e-+H2O===CH3COOH+4H+。下列有关说法正确的是( )
A.检测时,电解质溶液中的H+向负极移动
B.若有0.4 mol电子转移,则在标准状况下消耗4.48 L氧气
C.电池反应的化学方程式为CH3CH2OH+O2===CH3COOH+H2O
D.正极上发生的反应为O2+4e-+2H2O===4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
为了除去MgCl2的酸性溶液中的Fe3+,可在加热条件下加入一种试剂,过滤后再加入一定量的盐酸,这种试剂是( )
A.NH3·H2O B.NaOH C.Na2CO3 D.MgCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
有关麦芽糖的下列叙述中,错误的是( )
①纯净的麦芽糖是无色晶体,易溶于水,有甜味 ②麦芽糖能发生银镜反应,是一种还原性糖 ③1 mol麦芽糖发生水解得到1 mol葡萄糖和1 mol果糖 ④麦芽糖和蔗糖水解的产物完全相同
A.①② B.②③ C.③④ D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
星形聚合物SPLA可经下列反应路线得到(部分反应条件未注明)。
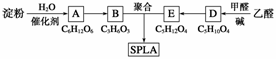
已知:SPLA的结构简式为
 ,其中R为
,其中R为
(1)淀粉是________糖(填“单”或“多”);A的名称是____________。
(2)乙醛由不饱和烃制备的方法之一是
________________________________________________________________________
________________________________________________________________________(用化学方程式表示,可多步)。
(3)D→E的化学反应类型属于________反应;D结构中有3个相同的基团,且1 mol D能与2 mol Ag(NH3)2OH反应,则D的结构简式是____________;D与银氨溶液反应的化学方程式为________________________________________________________________________
________________________________________________________________________。
(4)B的直链同分异构体G的分子中不含甲基,G既不能与NaHCO3溶液反应,又不能与新制Cu(OH)2悬浊液反应,且1 mol G与足量Na反应生成1 mol H2,则G的结构简式为________________________________________________________________________。
(5)B有多种脱水产物,其中两种产物的结构简式为____________________和
____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质间的反应既属于氧化还原反应,又属于离子反应的是( )
A.Zn与稀H2SO4
B.NaCl溶液与AgNO3溶液
C.H2与O2
D.Na2O与H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
现有部分前36号元素的性质或原子结构如下表:
| 元素编号 | 元素性质或原子结构 |
| R | 基态原子的最外层有3个未成对电子,次外层有2个电子 |
| S | 单质能与水剧烈反应,所得溶液呈弱酸性 |
| T | 基态原子3d轨道上有1个电子 |
| X |
|
(1)R元素的第一电离能要大于其同周期相邻的元素,原因是_____________。
(2)S元素的常见化合价为________,原因是__________________________。
(3)T元素的原子N能层上电子数为________。
(4)X的核外电子排布图违背了________。用X单质、碱金属盐及碱土金属盐等可以做成焰火。燃放时,焰火发出五颜六色的光,请用原子结构的知识解释发光的原因:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
水的电离平衡曲线如图所示:
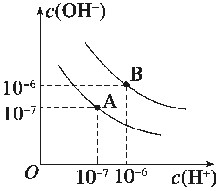
(1)若以A点表示25℃时水电离平衡时的离子浓度,当温度上升到100℃时,水的电离平衡状态到B点,则此时水的离子积从______增加到________。
(2)将pH=8的氢氧化钡溶液与pH=5的盐酸溶液混合并保持100℃恒温,欲使混合溶液的pH=7,则氢氧化钡溶液与盐酸的体积比为________。
(3)已知AnBm的离子积K=[c(Am+)]n·[c(Bn-)]m,式中c(Am+)和c(Bn-)表示离子的物质的量浓度。在某温度下,氢氧化钙溶解度为0.74 g,其饱和溶液密度设为1 g/cm3,其离子积为K=________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com