
用NA表示阿伏加德罗常数的值。下列叙述中不正确的是
A.16.9 g过氧化钡(BaO2)固体中阴、阳离子总数约为0.2NA
B.常温常压下,28 g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA
C.标准状况下,0.1molCl2溶于水,转移的电子数目小于0.1NA
D.某密闭容器盛有0.1 mol N2和0.3 mol H2,在一定条件下充分反应,转移电子的数目为0.6NA
D
【解析】
试题分析:A、16.9 g过氧化钡(BaO2)物质的量为:16.9 g÷169g/mol=0.1mol,因为O22为原子团,所以16.9 g过氧化钡(BaO2)固体中阴、阳离子总数约为0.2NA,故A正确;B、乙烯和环丁烷(C4H8)的最简式相同,为CH2,所以28 g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为28g÷14g/mol×NA mol-1=2NA,故B正确;C、Cl2部分与水反应,所以0.1molCl2溶于水,转移的电子数目小于0.1NA,故C正确;D、N2与H2的反应是可逆反应,所以0.1 mol N2和0.3 mol H2,在一定条件下充分反应,转移电子的数目小于0.6NA,故D错误。
考点:本题考查阿伏加德罗常数的计算。


科目:高中化学 来源:2014-2015陕西岐山县高一上学期期末质量检测化学试卷(解析版) 题型:计算题
(7分)向0.5 L0.04mol·L-1H2SO4溶液中加入一定量的CuO粉末,充分反应后,把50 g铁丝放入该溶液中,至铁丝质量不再变化时,共收集到224 mL气体(标准状况)。求:
(1)与硫酸反应的铁的物质的量;
(2)CuO粉末的质量。
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省濮阳市高二上学期第三次月考化学试卷(解析版) 题型:选择题
在0.1mol/L的CH3COOH溶液中存在如下电离平衡:CH3COOH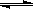 CH3COO-+H+,对于该平衡,下列叙述正确的是
CH3COO-+H+,对于该平衡,下列叙述正确的是
A.加入少量NaOH固体,平衡向逆反应方向移动
B.升高温度,平衡向正反应方向移动
C.加入水稀释,溶液中c(H+)一定增大
D.加入少量CH3COONa固体,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省弥勒市高三市统测一模理综化学试卷(解析版) 题型:选择题
下表中各组物质之间不能通过一步反应实现下图转化的是

甲 | 乙 | 丙 | |
A | AlCl3 | Al(OH)3 | Al2O3 |
B | SiO2 | H2SiO3 | Na2SiO3 |
C | Cl2 | HCl | NaCl |
D | CH2=CH2 | CH3CH2Cl | CH3CH2OH |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁省丹东五校协作体高三上学期期末考试理综化学试卷(解析版) 题型:选择题
短周期元素X、Y、Z、W的原子序数依次增大,X原子最外层电子数是其内层电子总数的3倍,Y原子最外层只有2个电子,Z单质可制成半导体材料,W与X属于同一主族。下列叙述正确的是
A.元素X的简单气态氢化物的热稳定性比W的弱
B.元素W的最高价氧化物对应水化物的酸性比Z的弱
C.原子半径的大小顺序:ry > rz > rw > rx
D.化合物YX、ZX2、WX3中化学键类型相同
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省景德镇市高三第二次质检理综化学试卷(解析版) 题型:填空题
(15分)甲醇是一种可再生能源,又是一种重要的化工原料,具有开发和应用的广阔前景。工业上可用如下方法合成甲醇:
方法一 | CO(g) +2H2(g) |
方法二 | CO2(g) +3H2(g) |
(1)已知:① 2CH3OH(l) + 3O2(g)  2CO2(g) + 4H2O(g) △H=-1275.6 kJmol-1
2CO2(g) + 4H2O(g) △H=-1275.6 kJmol-1
② 2CO(g) + O2(g)  2CO2(g) △H=-566.0 kJmol-1
2CO2(g) △H=-566.0 kJmol-1
③ H2O(l) = H2O(g) △H = + 44.0 kJmol-1
则甲醇不完全燃烧生成CO和液态水的热化学反应方程式为 。
(2)方法一生产甲醇是目前工业上常用的方法。在一定温度下,向2L密闭容器中充入1molCO和2molH2,发生上述反应,5分钟反应达平衡,此时CO的转化率为80%。请回答下列问题:
①前5分钟内甲醇的平均反应速率为 ;已知该反应在低温下能自发进行,则反应的
△H为 (填“>”、“<”或 “=”)0。
②在该温度下反应的平衡常数K= 。
③某时刻向该平衡体系中加入CO、H2、CH3OH各0.2mol后,将使ν正 ν逆(填“>”“=”“<”)。
(3)全钒液流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置,其原理如下图所示。
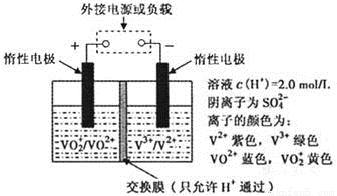
①当左槽溶液逐渐由黄变蓝,其电极反应式为 。
②充电过程中,右槽溶液颜色变化是 。
③若用甲醇燃料电池作为电源对其充电时,若消耗甲醇4.8g时,电路中转移的电量的为 (法拉第常数F=9.65×l04C · mol-1)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省景德镇市高三第二次质检理综化学试卷(解析版) 题型:选择题
现有1.0 mol/L的NaOH溶液0.2L,若通入4.48L(标准状况)SO2气体使其充分反应后,则所得溶液中各粒子浓度大小关系正确的是
A.c(Na+) = c(H2SO3) + c(HSO3―) + c ( H+)
B.c(SO32―) + c( OH―) = c(H+) + c(H2SO3)
C.c(Na+)+c(H+) = c(HSO3―) +c(SO32―) + c( OH―)
D.c(Na+)>c(HSO3―)>c( OH―)>c(H2SO3)>c(SO32―)>c(H+)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省镇江市高三第一学期期末调研测试化学试卷(解析版) 题型:选择题
下列有关实验装置(部分夹持装置已省略)进行的相应实验,能达到实验目的的是
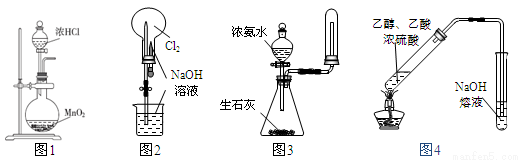
A.用图1所示装置可制取Cl2
B.用图2所示装置可完成“喷泉”实验
C.用图3所示装置可制取并收集干燥纯净的NH3
D.用图4所示装置可用于实验室制取乙酸乙酯
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省荆州市部分县市高三上学期期末统考理综化学试卷(解析版) 题型:填空题
[化学—选修2化学与技术](15分)
空气吹出法工艺是目前“海水提溴”的最主要方法之一,其工艺流程如下:

(1)目前,从海水中提取的溴约占世界溴年产量的 。
(2)步骤①中用硫酸酸化可提高Cl2的利用率,其原因是 。
(3)步骤④的离子方程式为 。
(4)步骤⑥的蒸馏过程中,溴出口温度要控制在8090℃。温度过高或过低都不利于生产,理由是 。
(5)步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差较大的特点进行分离。分离仪器的名称是 ,分离时液溴从分离器 (填“上口”或“下口")排出。
(6)不直接用含溴的海水进行蒸馏得到液溴,而要经过“空气吹出、S02吸收、氯化”的原因是 。
(7)某同学测得苦卤中溴的含量为0.8g/L,已知步骤①⑥中溴共损失了25%,步骤⑦和步骤⑧又共损失了所得溴蒸气的10%,若处理10 m3这样的苦卤,可得到液溴 mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com