
【题目】某有机物结构简式如下图所示,下列说法正确的是
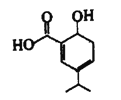
A. 分子式为C10H12O3 B. 能使酸性KMnO4溶液或溴水褪色
C. lmol该有机物可中和2molNaOH D. 1mol该有机物最多可与3molH2发生加成反应
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】10mLNO、CO2 的混合气体通过足量的Na2O2后,气体的体积变为6 mL (相同状况),则NO和CO2的体积比为( )
A.1:1B.2:1C.3:2D.1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可利用硫酸厂废渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁和绿矾(FeSO4·7H2O),聚铁的化学式可表示为[Fe2(OH)n(SO4)3-0.5n]m,主要工艺流程如下:
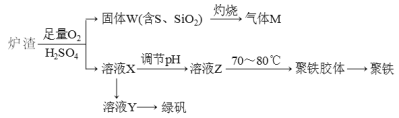
下列说法错误的是
A.炉渣中FeS与稀硫酸和氧气反应的离子方程式为:4FeS+3O2+12H+=4Fe3++4S↓+6H2O
B.气体M的成分是SO2,通入H2O2溶液得到硫酸,可循环使用
C.向溶液X中加入过量铁粉,充分反应后过滤得到溶液Y,再经蒸干即得绿矾
D.溶液Z的pH影响聚铁中铁的质量分数,若其pH偏小,将导致聚铁中铁的质量分数偏小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】网络趣味图片“一脸辛酸”,是在人脸上重复画满了辛酸的键线式结构(如图)。在辛酸的同分异构体中, 含有一个“-COOH”和三个“-CH3”的结构(不考虑立体异构),除![]() 外,还有( )
外,还有( )
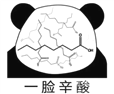
A. 7种 B. 11种 C. 14种 D. 17种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室有一份混有少量碳酸钙杂质的碳酸钡样品。分离并提纯碳酸钡的实验步骤如下[如图为Ba(OH)2和Ca(OH)2的溶解度曲线]:
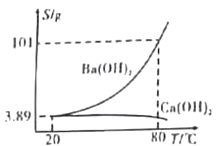
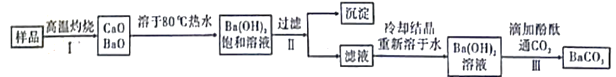
下列有关说法错误的是
A.步骤Ⅰ所需主要仪器是酒精喷灯、铁坩埚、泥三角、玻璃棒等
B.步骤Ⅱ中过滤时的温度对实验无明显影响
C.步骤Ⅲ中,当观察到红色刚好消失时,即可停止通CO2
D.上述过程中涉及到分解、化合、复分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝鞣剂主要成分为Al(OH)2Cl,主要用于揉制皮革。利用铝灰(主要成分为Al、Al2O3、AlN,FeO等)制备铝鞣剂的一种工艺如图所示:
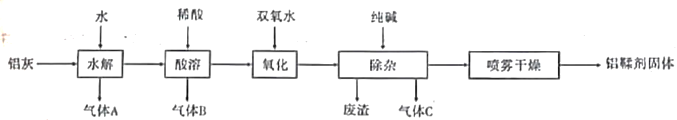
请回答下列问题:
(1)气体A、气体C的分子式为_________、______________
(2)产生气体B的化学方程式为:________________________________________________
(3)氧化时,发生反应的离子方程式为:__________________________________________
(4)废渣的主要成分为__________________(填化学式)。
(5)某同学设计如下方案测定铝鞣剂样品中Al(OH)2Cl质量分数。
操作Ⅰ:准确称取所制备的铝鞣剂m g放入烧杯中。
操作Ⅱ:加入_____________(填试剂名称),并用玻璃棒搅拌至固体全部溶解。
操作Ⅲ:加入足量___________(填化学式)溶液,充分反应,过滤、_________、__________得固体n g。根据所测数据即可计算出样品中Al(OH)2Cl质量分数。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨所需H2取自CH4,CH4和O2作用成CO2、H2(反应①),然而CH4和O2反应还能生成CO2、H2O(反应②),当有水生成时,H2O和CH4反应(反应③)。下表 为三个反应在不同温度下的平衡常数K。

(1)反应①的平衡常数K①的表达式为_______________。
(2)反应①②③的平衡常数K①、K②、K③之间的关系为K②=_____________(用含K①、 K③的式子表示)。反应①②③的反应焓变:ΔH①、ΔH②、ΔH③之间的关系为ΔH①= _____________(用含ΔH②、ΔH③的式子表示)。
(3)恒温条件下,反应③的能量与反应进程关系应对应下图中的_____________,反应② 的能量与反应进程关系应对应下图中的_____________。

(4)为使反应尽可能按生成H2的方向进行,若只考虑反应③,且不降低反应速率,可采 取__________措施;若只考虑反应①②,除采取控温措施外,还可采取_____________(写出两条措施即可)。
(5)250℃时,以镍合金为催化剂,发生CO2(g)+CH4(g)![]() 2CO(g)+2H2(g),向40L 的密闭容器中通入6molCO2(g)和6molCH4(g),平衡时测得体系中CH4的体积分数 为10%,则混合气体的密度为______g/L,CO2的转化率为__________(保留三位有效数字)。
2CO(g)+2H2(g),向40L 的密闭容器中通入6molCO2(g)和6molCH4(g),平衡时测得体系中CH4的体积分数 为10%,则混合气体的密度为______g/L,CO2的转化率为__________(保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,卤化银AgX(X:Cl-、Br-、I-)及Ag2CrO4的沉淀溶解平衡曲线如图所示。横坐标p(Ag+)表示“-lgc(Ag+)”,纵坐标Y表示“-lgc(X-)”或“-lgc(CrO42—)”。下列说法正确的是
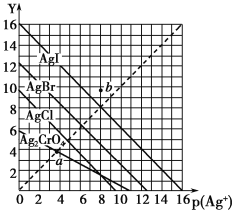
A. a点表示c(Ag+)=c(CrO42—)
B. b点可表示AgI的饱和溶液
C. 该温度下AgI的Ksp约为1×10-16
D. 该温度下AgCl、AgBr饱和溶液中:c(Cl-)<c(Br-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有 8 种元素的性质、数据如下表所列,它们属于第二或第三周期。
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
-2 | -3 | -1 | -3 |
回答下列问题:
(1)④的元素名称是_____,⑧的元素符号是_____。②在元素周期表中的位置是(周期、族)_____ 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是_____;名称是________; 碱性最强的化合物的电子式是:_________; 属_____化合物(填“离子”或“共价”)。
(3)①的最简单氢化物的电子式为_____, ⑦的最简单氢化物的电子式为_____,结构式为_____。
(4)写出⑦的最高价氧化物对应水化物跟它的氢化物反应的化学方程式:_________________ 。
(5)写出②最高价氧化物对应水化物跟⑤的氢化物水溶液反应的离子方程式:____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com