
【题目】硅及其化合物在材料领域中的应用广泛.下列叙述不正确的是( )
A. 硅单质可用来制造太阳能电池
B. 二氧化硅是制造光导纤维的材料
C. 石英(SiO2)可用来制作工艺品
D. 硅单质是制造玻璃的主要原料
科目:高中化学 来源: 题型:
【题目】某化学研究性学习小组设想探究铜的常见化学性质,过程设计如下:
[提出猜想]
问题1:在周期表中,铜与铝的位置很接近,铜不如铝活泼,氢氧化铝具有两性,氢氧化铜有两性吗?
问题2:铁和铜都有变价,一般情况下,正二价铁的稳定性小于正三价的铁,正一价的铜稳定性也小于正二价的铜吗?
问题3:氧化铜有氧化性,能被H2、CO还原,它能被氮的某种气态氢化物还原吗?
[实验探究]
Ⅰ.解决问题1:
(1)需用到的药品除铜、铝、1mol/LCuSO4溶液、稀H2SO4外还需___________ (填试剂化学式);
(2)配制1 mol/LCuSO4溶液25mL,选用的仪器除烧杯、天平、玻璃棒、量筒、胶头滴管外,还有_________________(填仪器名称);
(3)为达到目的,你认为应进行哪些相关实验?(实验内容和步骤)
①制备Cu(OH)2; ②_______________________________________________________
Ⅱ.解决问题2的实验步骤和现象如下:取一定量制得的氢氧化铜周体,于坩埚中灼烧,当温度达到80~100℃得到黑色同体粉末;继续加热至1000℃以上,黑色粉末全部变成红色粉末氧化亚铜;取适量红色氧化亚铜粉末于洁净试管中,加入过量的稀硫酸或盐酸,得到蓝色溶液,同时观察到试管底还有红色固体存在。根据以上实验及现象:
(4)写出氧化亚铜与稀硫酸(或盐酸)反应的离子方程式:_________________________________;
(5)从实验Ⅱ可得出的结论是__________________________________________________________。
Ⅲ.解决问题3:
设计如下装置:(夹持装置未画出)
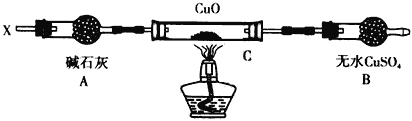
当某种氮的气态氢化物(X)缓缓通过灼热的氧化铜,观察到氧化铜由黑色变成了红色,无水硫酸铜变成蓝色,生成物中还有一种无污染的气体Y;将X通入红热的CuO燃烧管完全反应后,消耗0.01 mol X,测得B装置增重0.36 g,并收集到单质气体Y0.28 g;
(6)研究小组同学确证燃烧管生成的红色物质是铜,你认为他们确证的方法是________________;
(7)X气体的摩尔质量为_____________;
(8)C中发生反应的化学方程式:______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】航天飞船可用肼(N2H4)作动力源。已知1 g液态肼和足量的液态过氧化氢反应生成N2和水蒸气时放出20.05 kJ热量,化学方程式为N2H4+2H2O2=N2↑+4H2O。下列说法中错误的是 ( )
A. 肼(N2H4)分子中只存在极性共价键
B. 此情况下,液态肼燃烧生成1 mol N2时放出的热量为641.6 kJ
C. 该反应中肼作还原剂
D. 该反应的反应物总能量高于生成物的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在固定体积的密闭容器中发生下列反应:2HI![]() H2+I2。若c(HI)由0.1 mol·L-1降到0.07 mol·L-1时,需要15 s,那么c(HI)由0.07 mol·L-1降到0.05 mol·L-1时,所需反应的时间为 ( )
H2+I2。若c(HI)由0.1 mol·L-1降到0.07 mol·L-1时,需要15 s,那么c(HI)由0.07 mol·L-1降到0.05 mol·L-1时,所需反应的时间为 ( )
A. 5 sB. 10 sC. 大于10 sD. 小于10 s
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将气体A、B置于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g)![]() 2C(g)+2D(g),反应进行到10 s末达到平衡,此时测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
2C(g)+2D(g),反应进行到10 s末达到平衡,此时测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
(1)用C表示10 s内反应的平均反应速率为________。
(2)10 s末,生成物D的浓度为________。
(3)A与B的平衡转化率之比为________。
(4)反应过程中容器内气体的平均相对分子质量变化是_____(填“增大”、“减小”或“不变”,下同),气体的密度变化是______。
(5)在一定温度下,体积不变的密闭容器中,上述反应达到平衡的标志是_______(填字母)。
A. 气体总质量保持不变 B. A、B、C、D的浓度都相等
C. 每消耗3 mol A的同时生成2 mol D D. A、B、C、D的分子数之比为3∶1∶2∶2
E. 3V正(A) = 2V逆(C) F. A的转化率保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据图中包含的信息分析,下列叙述正确的是 ( )
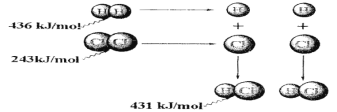
A.氢气与氯气反应生成1 mol氯化氢气体,反应吸收248 kJ的能量
B.436 kJ/mol是指断开1 mol H2中的H-H键需要放出436 kJ的能量
C.氢气与氯气反应生成2 mol氯化氢气体,反应放出183 kJ的能量
D.431kJ/mol是指生成2 mol HCl中的H-Cl键需要放出431 kJ的能量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com