
| A. | 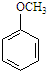 | B. |  | C. | 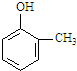 | D. | 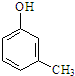 |
分析 化合物的核磁共振氢谱中出现5个峰说明有机物中含有5种类型的氢原子,根据等效氢判断;分子中等效氢原子一般有如下情况:①分子中同一甲基上连接的氢原子等效,②同一碳原子所连甲基上的氢原子等效,③处于镜面对称位置上的氢原子等效.
解答 解:核磁共振氢谱中出现5个峰说明有机物中含有5种类型的氢原子,
A. 中苯环有3种H原子,侧链的甲基上有1种H原子,故分子中含有4种H原子,故A错误;
中苯环有3种H原子,侧链的甲基上有1种H原子,故分子中含有4种H原子,故A错误;
B. 中苯环上有3种H原子,侧链的亚甲基上有1种H原子,羟基上有1种H原子,故分子中含有5种H原子,故B正确;
中苯环上有3种H原子,侧链的亚甲基上有1种H原子,羟基上有1种H原子,故分子中含有5种H原子,故B正确;
C. 分子中,苯环上有4种H原子,侧链的甲基上有1种H原子,羟基上有1种H原子,故分子中含有6种H原子,故C错误;
分子中,苯环上有4种H原子,侧链的甲基上有1种H原子,羟基上有1种H原子,故分子中含有6种H原子,故C错误;
D. 分子中,苯环上含有4种H,甲基和羟基各含有1种H原子,总共含有6种H原子,故D错误;
分子中,苯环上含有4种H,甲基和羟基各含有1种H原子,总共含有6种H原子,故D错误;
故选B.
点评 本题考查有机物结构及核磁共振氢谱,题目难度不大,明确常见有机物结构为解答根据,注意掌握核磁共振氢谱的含义及应用方法,试题培养了学生灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钡的电离方程式为Ba(OH)2=Ba2++2OH- | |
| B. | 强弱电解质的本质区别是溶液的导电性强弱 | |
| C. | 电解质与非电解质的本质区别是水溶液能否导电 | |
| D. | 硫酸氢钠是强电解质,碳酸氢钠是弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向NaOH溶液中慢慢滴加FeCl3饱和溶液,可制得Fe(OH)3胶体 | |
| B. | 胶体与其他分散系的本质区别是胶体能发生丁达尔效应 | |
| C. | 分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 纯碱和烧碱都属于碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100 ml 容量瓶、40 g | B. | 500 ml 容量瓶、40 g | ||
| C. | 100 ml 容量瓶、80 g | D. | 500 ml 容量瓶、80 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl KCl | B. | CO2 SiO2 | C. | NH4Cl CCl4 | D. | NaOH Na2O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com