
���� ������ǿ�������Σ�������ˮ�����Һ�ʼ��ԣ�
��1�������ƣ�Na2Sx�������Ը��������Һ��Ӧ���������������Ϊ�����ƣ����������������ԭ��Mn2+����Ԫ�صĻ��ϼ۱仯����ת�Ƶĵ�������ȷ����������x���Ӷ�ȷ���仯ѧʽ��
��2��Na2S��Һ�ڿ����г��ڷ��ã���������Ӧ�������������ɶ����ƣ�SԪ�صĻ��ϼ���-2�۱�Ϊ-1�ۣ�
��3��Na2S2����Һ�����ᷴӦ�����Ȼ��ơ�S�����⣮
��� �⣺������ǿ�������Σ�������ˮ�����Һ�ʼ��ԣ�ˮ�ⷽ��ʽΪ��S2-+H2O?HS-+OH-��HS-+H2O?H2S+OH-��
�ʴ�Ϊ��S2-+H2O?HS-+OH-��HS-+H2O?H2S+OH-��
��1�����������Һ��Ӧ������ԭ��Mn2+��Mn��+7��+2����Na2Sx�������������Ϊ�����ƣ�S��-$\frac{2}{x}$��+6�����ɵ����غ��֪100mL��4mol•L-1��[+6-��-$\frac{2}{x}$��]��x=200mL��1.4mol•L-1��[+7-��+2��]����ã�x=5�����Ի�ѧʽΪ��Na2S2��
�ʴ�Ϊ��Na2S2��
��2��Na2S��������ˮ��Ӧ����Na2S2��NaOH���÷�Ӧ�ķ���ʽΪ4Na2S+O2+2H2O�T4NaOH+2Na2S2��
�ʴ�Ϊ��4Na2S+O2+2H2O�T4NaOH+2Na2S2��
��3�������������ᷴӦ�������г�������ζ������ΪH2S��dz��ɫ����ΪS�����ӷ���ʽΪ��S22-+2H+=H2S��+S����
�ʴ�Ϊ��S22-+2H+=H2S��+S����
���� ���⿼�����ӵ�ˮ�⡢������ԭ��Ӧ��Ϊ�߿���Ƶ���㣬���շ�Ӧ��Ԫ�صĻ��ϼ۱仯Ϊ���Ĺؼ���ע�⻯�ϼ���Ԫ�ص����ʼ�ϰ���е���Ϣ����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na2CO3 | B�� | Na2SO4 | C�� | Al2O3 | D�� | Al |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
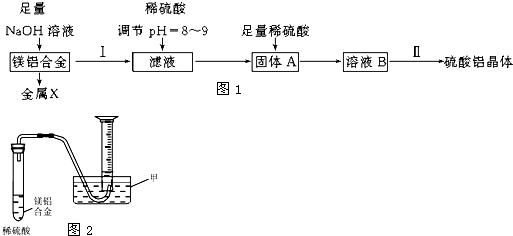
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | N2 | B�� | CO2 | C�� | H2 | D�� | O2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��ѧ�� | Cl-Cl | PCl3��P-Cl�� | PCl5��P-Cl�� |
| ����/kJ•mol-1 | d | 1.2c | c |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��ͼ��ʾ����֪��ƿ�ݻ���ͬ��ͬ��ͬѹ�£���ƿ�ڳ����Ȼ������壬����ƿ�г������л�������е�ijһ��ʱ��������ԭ����������ƿ������ԭ������һ����ȣ���û�������ǣ�������
��ͼ��ʾ����֪��ƿ�ݻ���ͬ��ͬ��ͬѹ�£���ƿ�ڳ����Ȼ������壬����ƿ�г������л�������е�ijһ��ʱ��������ԭ����������ƿ������ԭ������һ����ȣ���û�������ǣ�������| A�� | O3��N2 | B�� | CH4��NH3 | C�� | N2��O2 | D�� | CO��CO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��2 | B�� | 2��l | C�� | 3��2 | D�� | 2��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | 1��1��1 | B�� | 2��1��1 | C�� | 1��2��1 | D�� | 1��1��3 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com