
A、B、C三只烧杯中,依次分别盛有NaOH溶液、KSCN溶液、煮沸的蒸馏水,各滴入FeCl3溶液,试根据实验现象分别回答以下问题:
(1)分别写出三只烧杯中形成分散系的名称:A_____,B____,C____。
(2)写出A中形成分散系的离子方程式:_________。
(3)写出C中形成分散系的化学方程式:_________。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
现有下列仪器:①集气瓶;②量筒;③烧杯;④表面皿;⑤蒸发皿;⑥容量瓶;⑦圆底烧瓶。其中能用
酒精灯加热的是 ( )
A.②③⑤ B.③⑥⑦ C.①③④ D.③⑤⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物X,它的氧化产物甲和还原产物乙都能和金属钠反应放出H2。甲和乙反应可生成丙,甲和丙均能发生银镜反应。这种有机物X是
A.甲醇 B.甲醛 C.甲酸 D.甲酸甲酯
查看答案和解析>>
科目:高中化学 来源: 题型:
下列图中的实验方案,能达到实验目的的是( )
| A | B | C | D | |
| 实验方案 |
|
将NO2球浸泡在冰水和热水中 |
|
|
| 实验 目的 | 验证FeCl3对H2O2分解反应有催化作用 | 探究温度对平衡 2NO2 | 除去CO2气体中混有的SO2 | 比较HCl、H2CO3和H2SiO3的酸性强弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究小组同学为探究Fe3+能否氧化SO2,设计了如下的实验装置(假设实验中所用装置的气密性良好)。
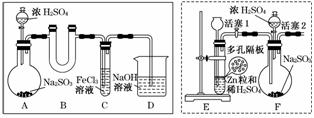
(1)甲同学利用实线框内的装置制取SO2,并进行探究实验。
①装置A中发生反应的化学方程式为_________________________________________。
②装置B的作用是________________________________________________________。
③反应一段时间后,甲同学取出装置C中的少量溶液,向其中加入盐酸酸化的BaCl2溶液,观察到有白色沉淀生成。由此得出结论:Fe3+可以氧化SO2。
(2)乙同学认为甲同学的实验不严谨,用虚线框内的装置代替装置A,先让装置E内的试剂反应一段时间后,关闭活塞1,打开活塞2,又反应片刻后,取装置C中的少量溶液,向其中加入酸性KMnO4溶液,观察到KMnO4溶液紫红色褪去。由此得出结论:Fe3+可氧化SO2,且可被SO2还原成Fe2+。
①该实验制取H2时需用浓硫酸配制450 mL 3 mol·L-1的稀硫酸,所需的玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管外,还需用到______________________________________。
配制过程中若其他操作无误,但没有洗涤烧杯与玻璃棒,则所配制溶液的浓度会___ _____(填“偏高”、“偏低”或“无影响”)。
②在该实验过程中,H2所起的作用是________________________________________。
(3)丙同学认为甲、乙两位同学的实验均不严谨,为此利用乙同学的实验装置及操作重新进行实验。待装置F内的试剂反应一段时间后,取装置C中的少量溶液,向其中加入盐酸酸化的BaCl2溶液,得出与甲同学相同的结论。
①甲同学实验不严谨的原因是________(填序号)。
A.SO2的溶解度太小
B.SO2与Fe3+不发生反应
C.H2SO3与BaCl2溶液不反应
D.装置中的空气与SO2进入水中可生成H2SO4
②乙同学的实验结论不严谨的原因是___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
CO2的的资源化利用是解决温室效应的重要途径。以下是在一定条件下用NH3捕获CO2生成重要化工产品三聚氰胺的反应:NH3+CO2→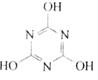 +H2O。下列有关三聚氰胺的说法正确的是
+H2O。下列有关三聚氰胺的说法正确的是
A.分子式为C3H6N3O3  B.分子中既含极性键,又含非极性键
B.分子中既含极性键,又含非极性键
C.属于共价化合物 D .生
.生 成该物质的上述反应为中和反应
成该物质的上述反应为中和反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质的性质与应用相对应的是 (  )
)
A.NH3极易溶于水,可用作制冷剂
B.Al2O3熔点高,可用作耐高温材料
C.SO2具有氧化性,可用于漂白品红、织物等
D.BaCO3能与盐酸反应,可用于治疗胃酸过多
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA表示阿伏加德罗常数,下列叙述中正确的是 ( )
A.常温常压下,48gO3含有的氧原子数为3NA
B.1.8g的NH4+离子中含有的电子数为1.1NA
C.常温常压下,11.2L氧气所含的原子数为NA
D.2.4g金属镁变为镁离子时失去的电子数为0.1NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com