
����Ŀ����ͭƬ��пƬ��200mLϡH2SO4��ɵ�ԭ����У���ͼ��ʾװ�ã����밴Ҫ����գ�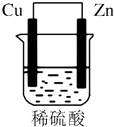
��1��Ϊ������������Ӧ������������ԭ������������ �� �缫��ӦʽΪ��Ϊ������������Ӧ������������ԭ������������ �� �缫��ӦʽΪ ��
��2��H+�����ƶ���������������Ϊ�����ߡ�����缫���ϣ�
��3����пƬֻ�����绯ѧ��Ӧ����ͭƬ�Ϲ��ų�3.36L����״��������ʱ��H2SO4ǡ����ȫ���ģ���
�ٷ�Ӧ�����ĵ�п������
����������ͨ���˵��ߣ�
��ԭϡH2SO4�����ʵ���Ũ���� ��
���𰸡�
��1��Cu����ԭ�����������ɣ�2H++2e���TH2����Zn��������п���ܽ⣻Zn��2e���TZn2+
��2��Cu��Zn��Cu
��3��9.75g��0.3NA��1.5mol/L
���������⣺��1���γ�ԭ���ʱ��ͭΪԭ���������������ԭ��Ӧ���缫����ʽΪ2H++2e���TH2������Cu�����������ɣ�пΪ���������ܽ⣬пʧ���ӷ���������Ӧ���缫����ʽΪZn��2e���TZn2+ �� ���Դ��ǣ�Cu����ԭ�����������ɣ�2H++2e���TH2����Zn��������п���ܽ⣻Zn��2e���TZn2+����2��CuΪ������ZnΪ��������Һ���������������ƶ��������ɸ�����������������Zn������Cu�������Դ��ǣ�Cu��Zn��Cu����3��ͭ�缫����ʽΪ2H++2e���TH2����n��H2��= ![]() =0.15mol��ת��0.3mol���ӣ�����֪�缫����ʽΪZn��2e���TZn2+ �� ת��0.3mol���ӣ�����0.15molп�������ĵ�пΪ0.15mol��65mol/L=9.75g�����Դ��ǣ�9.75g����ת�Ƶĵ�����Ϊ0.3NA�������Դ��ǣ�0.3NA����������ȫ���ģ���n��H2��=n��H2SO4������ԭ����������ʵ���Ϊ0.15mol��
=0.15mol��ת��0.3mol���ӣ�����֪�缫����ʽΪZn��2e���TZn2+ �� ת��0.3mol���ӣ�����0.15molп�������ĵ�пΪ0.15mol��65mol/L=9.75g�����Դ��ǣ�9.75g����ת�Ƶĵ�����Ϊ0.3NA�������Դ��ǣ�0.3NA����������ȫ���ģ���n��H2��=n��H2SO4������ԭ����������ʵ���Ϊ0.15mol��
����ԭ��������ʵ���Ũ����c= ![]() =
= ![]() =0.75mol/L�����Դ��ǣ�0.75mol/L��
=0.75mol/L�����Դ��ǣ�0.75mol/L��


 Ӧ�����������Ĵ���ѧ������ϵ�д�
Ӧ�����������Ĵ���ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������¶�ʱ����ѧ��Ӧ���ʼӿ�ԭ��ĺ���������
A.�û�ѧ��Ӧ�Ĺ��������ȵ�
B.�û�ѧ��Ӧ�Ĺ����Ƿ��ȵ�
C.�����˶����ʼӿ죬ʹ��Ӧ����ӵ���ײ��������
D.��Ӧ����ӵ��������ӣ�����Ӱٷ������ӣ���Ч��ײ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ����ʵ��װ�ã��ֱ�ش��������⣮ 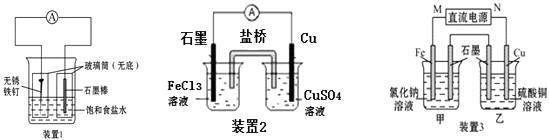
��1��װ��1Ϊ����������ʴʵ�飮һ��ʱ��������ʯī���IJ���Ͳ�ڵ����̪��Һ���ɹ۲쵽ʯī����������Һ��죬���װ����ʯī�缫�ķ�ӦʽΪ ��
��2��װ��2�е�ͭ���������������������װ����ʯī�缫�������ķ�ӦΪ ��
��3��װ��3�м��ձ�ʢ��100mL 0.2molL��1��NaCl��Һ�����ձ�ʢ��100mL0.5molL��1��CuSO4��Һ����Ӧһ��ʱ���ֹͣͨ�磮����ձ��е��뼸�η�̪���۲쵽ʯī�缫�������ȱ�죮
�ټ��ձ�����Ϊ�������ձ���ʯī�缫�ĵ缫��ӦʽΪ ��
�����ձ��е�ⷴӦ�����ӷ���ʽΪ ��
��ֹͣ��⣬ȡ��Cu�缫��ϴ�ӡ�����������缫����0.64g�����ձ��в����������ڱ�״���µ����ΪmL��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾʵ��װ�õ�K�պϣ������ж���ȷ����
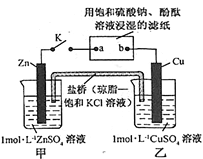
A. Ƭ�̺�׳���c(SO42�� )����
B. ������Zn��a��b��Cu·������
C. Ƭ�̺��ҳ���c(Cu2 + )����
D. Ƭ�̺�ɹ۲쵽��ֽa����ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڷ�ӦCO(g)+H2O(g)![]() CO2(g)+H2(g) ��H<0����������������������( )
CO2(g)+H2(g) ��H<0����������������������( )
A. ����������ı��˷�Ӧ��;������Ӧ����HҲ��֮�ı�
B. �ı�ѹǿ��ƽ�ⲻ�����ƶ�����Ӧ�ų�����������
C. �����¶ȣ���Ӧ���ʼӿ죬��Ӧ�ų�����������
D. ����ԭ����н��У���Ӧ�ų�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����н����ķ�����������ȷ���� (����)
A.�Խ�������Ϳ�����Է�ֹ����
B.������п��ķ�������������
C.��ijЩ���ߵ�����еת����λ��ѡ��ˢ����ķ���������
D.�ڵ������͵��������Ͻ�ֱ����Դ�ĸ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��ѧ��Ҫ������ѧר�����������������л�ѧ����ʹ����ȷ���ǣ� ��
A.������̼���ӵĽṹʽΪ O��C��O
B.�����Ƶĵ���ʽ�� ![]()
C.Fԭ�ӵĽṹʾ��ͼ�� ![]()
D.�õ���ʽ��ʾ�Ȼ�����ӵ��γɹ��̣� ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA���������ӵ�������ֵ������������ȷ����
A. 1L 0.1mol��L��1��NaHCO3��Һ��HCO3����CO32��������֮��Ϊ0.1NA
B. 60g�����д��ڵĹ��ۼ�����Ϊ10NA
C. ����������ˮ��Ӧʱ������0.1mol����ת�Ƶĵ�����Ϊ0.2NA
D. 235g![]() U�����ѱ䷴Ӧ��
U�����ѱ䷴Ӧ�� ![]() U+
U+![]() n
n![]()
![]() Sr+
Sr+![]() U+10
U+10![]() n������������(
n������������(![]() n)��Ϊ10NA
n)��Ϊ10NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ΪӪ����������������,�������ڷ�����Ҫ�ķ�Ӧ�� �� ��
A. ������Ӧ B. ȡ����Ӧ C. �ӳɷ�Ӧ D. �Ӿ۷�Ӧ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com