
| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
分析 ①某些元素自然界中不含有游离态;
②离子可分成原子;
③分子是保持这种物质化学性质的最小粒子;
④电子的质量可忽略不计;
⑤由同一种元素组成的物质可能含多种物质;
⑥质子数、中子数和电子数都相同的微粒不一定是同一种粒子;
⑦碱性氧化物都是金属氧化物;
⑧和碱反应生成盐和水的氧化物为酸性氧化物.
解答 解:①某些元素自然界中不含有游离态,如硅元素、钠元素等,故①错误;
②离子可分成原子,可再分,故②错误;
③物质的化学性质不一定不由分子保持的,如二氧化硅,故③错误;
④电子的质量可忽略不计,原子与该原子形成的简单离子相对质量几乎相等,故④正确;
⑤某物质经实验测定只含一种元素,不一定是纯净物,如氧气和臭氧,只有一种元素,O元素,但是混合物,故⑤错误;
⑥质子数、中子数和电子数都相同的微粒不一定是同一种粒子,如铵根离子和钠离子,故⑥错误;
⑦碱性氧化物都是金属氧化物,但金属氧化物不一定是碱性氧化物,如Mn2O7,故⑦正确;
⑧和碱反应生成盐和水的氧化物为酸性氧化物,可以是金属氧化物如Mn2O7,故⑧正确.
故选A.
点评 本题考查了物质分类的方法和物质结构分析,概念的实质理解是解题关键,题目难度不大,学习中注意相关基础知识的积累.


科目:高中化学 来源: 题型:选择题
| A. | 由ZR组成的化合物为离子化合物 | B. | 含氧酸酸性R>X | ||
| C. | X、Y只能共存于共价化合物中 | D. | 原子半径Z>R>Y>X |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子最外层电子数由少到多的顺序:X=W<Y<Z | |
| B. | 原子半径由大到小的顺序:r(W)>r(X)>r(Y)>r(Z) | |
| C. | 元素非金属性由强到弱的顺序:X、Y、W | |
| D. | 元素的简单气态氢化物的稳定性由强到弱的顺序:Y、X、W |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
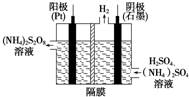 (1)过二硫酸铵法(如图所示)是目前最流行的制备H2O2的方法.即电解含H2SO4、(NH4)2SO4的溶液制取(NH4)2S2O8,再与热水反应即可得H2O2和(NH4)2SO4.
(1)过二硫酸铵法(如图所示)是目前最流行的制备H2O2的方法.即电解含H2SO4、(NH4)2SO4的溶液制取(NH4)2S2O8,再与热水反应即可得H2O2和(NH4)2SO4.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤⑥⑦ | B. | ①②⑤⑦⑧ | C. | ②③④⑤⑥ | D. | ①③⑥⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4:1 | B. | 1:4 | C. | 1:6 | D. | 6:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
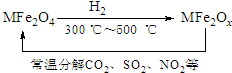 新型纳米材料氧缺位铁酸盐MFe2Ox(3<x<4,M=Mn、Zn、Ni,且均为+2价,下同)是由铁酸盐MFe2O4经过高温与H2反应制得.常温下,它能使工业废气中的酸性氧化物(SO2、NO2等)转化为其单质除去,转化流程如图:
新型纳米材料氧缺位铁酸盐MFe2Ox(3<x<4,M=Mn、Zn、Ni,且均为+2价,下同)是由铁酸盐MFe2O4经过高温与H2反应制得.常温下,它能使工业废气中的酸性氧化物(SO2、NO2等)转化为其单质除去,转化流程如图:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | 目的 | 操作 |
| A | 配置100mL 1.0mol•L-1CuSO4溶液 | 将25gCuSO4•5H2O溶于100mL蒸馏水中 |
| B | 除去KNO3固体中少量NaCl | 将混合物制成熟的饱和溶液,冷却结晶,过滤 |
| C | 提取溴水中的Br2 | 向溶液中加入乙醇后振荡,静置,分液 |
| D | 检验溶液中是否含有NH4+ | 取少量溶液于试管中,加入NaOH后,加热,在试管口放置 一块湿润的红色石蕊试纸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com