
| A. | 称量10.56gNa2CO3固体--用托盘天平 | |
| B. | 准确量取10.00mL的溶液--用50mL量筒 | |
| C. | 灼烧干海带至完全变成灰烬--用蒸发皿 | |
| D. | 过滤煮沸后的硬水--用普通漏斗 |
分析 A.托盘天平的感量为0.1g;
B.量筒的感量为0.1mL;
C.灼烧在坩埚中进行;
D.煮沸后的硬水,钙、镁离子转化为沉淀.
解答 解:A.托盘天平的感量为0.1g,则可称量10.5g或10.6gNa2CO3固体,故A错误;
B.量筒的感量为0.1mL,则可用10mL量筒量取10.0mL的溶液,故B错误;
C.灼烧在坩埚中进行,不能在蒸发皿中进行,蒸发皿用于可溶性固体与液体的分离,故C错误;
D.煮沸后的硬水,钙、镁离子转化为沉淀,则利于普通漏斗过滤可分离,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握仪器的使用、实验基本操作、混合物分离提纯为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


科目:高中化学 来源: 题型:选择题
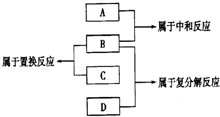 现有A B C D四种物质,他们分别为铁、盐酸、氢氧化钠溶液、硝酸银溶液四种物质中一种,它们之间反应关系及所发生的反应类型如图,下列物质对应正确的是( )
现有A B C D四种物质,他们分别为铁、盐酸、氢氧化钠溶液、硝酸银溶液四种物质中一种,它们之间反应关系及所发生的反应类型如图,下列物质对应正确的是( )| A. | A铁 | B. | B盐酸 | C. | C氢氧化钠溶液 | D. | D硝酸银溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 沸点:H2S>H2Se | B. | 熔点:NaCl>CCl4 | ||
| C. | 酸性:HClO4>H2SO4 | D. | 碱性:NaOH>Mg(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用25 mL量筒量取12.36 mL盐酸 | |
| B. | 用pH试纸测出某溶液pH为3.5 | |
| C. | 用托盘天平称取8.75 g食盐 | |
| D. | 用酸式滴定管测出消耗盐酸的体积为15.60 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com