
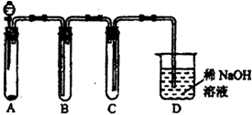
 请回答下列实验室中制取气体的有关问题.
请回答下列实验室中制取气体的有关问题.
| 应加入的物质 | 所起的作用 | |
| A | ______ | ______ |
| B | ______ | ______ |
| C | ______ | ______ |
| D | ______ | ______ |
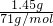 ,则m(KMnO4)=
,则m(KMnO4)=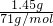 ×
×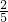 ×158g/mol=1.29g,反应中发生转移的电子的物质的量为
×158g/mol=1.29g,反应中发生转移的电子的物质的量为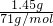 ×2=0.04mol,
×2=0.04mol,| 应加入的物质 | 所起的作用 | |
| A | 铜屑和稀硝酸 | 产生NO气体 |
| B | 水 | 排水收集NO气体 |
| C | 接收B中排出的水 | |
| D |


科目:高中化学 来源: 题型:阅读理解

| 浓硫酸 |
| 加热 |
| 浓硫酸 |
| 加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某兴趣小组同学在实验室用加热l-丁醇、浓H2SO4和溴化钠混合物的方法来制备1-溴丁烷,设计了如图所示的实验装置(其中的夹持仪器没有画出).
某兴趣小组同学在实验室用加热l-丁醇、浓H2SO4和溴化钠混合物的方法来制备1-溴丁烷,设计了如图所示的实验装置(其中的夹持仪器没有画出).| 浓硫酸 |
| 加热 |
| 浓硫酸 |
| 加热 |
| 物质 | 熔点/℃ | 沸点/℃ |
| 1-丁醇 | -89.5 | 117.3 |
| 1-溴丁烷 | -112.4 | 101.6 |
| 丁醚 | -95.3 | 142.4 |
| 1-丁烯 | -185.3 | -6.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 乙醇 | 溴乙烷 | 正丁醇 | 1-溴丁烷 | |
| 密度/g?cm-3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
| 沸点/℃ | 78.5 | 38.4 | 117.2 | 101.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| 物理性质 | 乙酸 | 乙醇 | 1-丁醇 | 乙酸乙酯 | 乙酸丁酯 |
| 熔点(℃) | 16.6 | -117.3 | -89.5 | -83.6 | -73.5 |
| 沸点(℃) | 117.9 | 78.5 | 117 | 77.06 | 126.3 |
| 密度(g/cm3) | 1.05 | 0.79 | 0.81 | 0.90 | 0.88 |

查看答案和解析>>
科目:高中化学 来源: 题型:
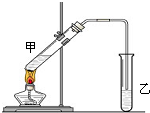 俗话说,“陈酒老醋特别香”,其原因是酒在储存过程中生成了有香味的乙酸乙酯,在实验室里我们也可以用如图所示的装置来模拟该过程.请回答下列问题:
俗话说,“陈酒老醋特别香”,其原因是酒在储存过程中生成了有香味的乙酸乙酯,在实验室里我们也可以用如图所示的装置来模拟该过程.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com