
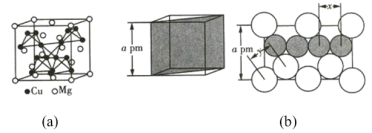
【题目】(1)图(a)是MgCu2的拉维斯结构,Mg以金刚石方式堆积,八面体空隙和半数的四面体空隙中,填入以四面体方式排列的Cu。图(b)是沿立方格子对角面取得的截图。可见,Cu原子之间最短距离x=_________pm,Mg原子之间最短距离y=_________pm。设阿伏加德罗常数的值为NA,则MgCu2的密度是_________g·cm-3(列出计算表达式)。
(2)一种四方结构的超导化合物的晶胞如图1所示。晶胞中Sm和As原子的投影位置如图2所示。图中F-和O2-共同占据晶胞的上下底面位置,若两者的比例依次用x和1-x代表,则该化合物的化学式表示为__________;通过测定密度![]() 和晶胞参数,可以计算该物质的x值,完成它们关系表达式:ρ=____g·cm-3。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图1中原子的坐标为(
和晶胞参数,可以计算该物质的x值,完成它们关系表达式:ρ=____g·cm-3。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图1中原子的坐标为(![]() ,
,![]() ,
,![]() )则原子2和3的坐标分别为__________、__________。
)则原子2和3的坐标分别为__________、__________。

【答案】![]()
![]()
![]() SmFeAsO1-xFx
SmFeAsO1-xFx 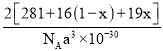 (
(![]() ,
,![]() ,0) (0,0,
,0) (0,0,![]() )
)
【解析】
(1)如图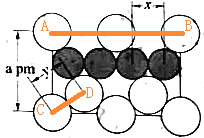 所示,AB之间的距离为面对角线长度=
所示,AB之间的距离为面对角线长度=![]() a pm,AB之间距离相当于4个Cu原子直径,x距离1个Cu原子直径=
a pm,AB之间距离相当于4个Cu原子直径,x距离1个Cu原子直径=![]() pm,体对角线长度=
pm,体对角线长度=![]() 棱长=
棱长=![]() a pm;CD距离为y,该长度为体对角线BC长度的
a pm;CD距离为y,该长度为体对角线BC长度的![]() =
=![]() ×
×![]() a pm=
a pm=![]() pm,该晶胞中Mg原子位于8个顶点上、6个面心上,在晶胞内部有4个Mg原子,所以Mg原子个数=8×
pm,该晶胞中Mg原子位于8个顶点上、6个面心上,在晶胞内部有4个Mg原子,所以Mg原子个数=8×![]() +6×
+6×![]() +4=8,Cu原子都位于晶胞内部,有16个;晶胞体积V=(a×10-10 cm)3,晶胞密度ρ=
+4=8,Cu原子都位于晶胞内部,有16个;晶胞体积V=(a×10-10 cm)3,晶胞密度ρ=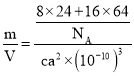 g/cm3=
g/cm3=![]() g/cm3;
g/cm3;
(2)由晶胞结构中各原子所在位置可知,该晶胞中Sm个数为![]() ,Fe个数为
,Fe个数为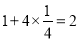 ,As个数为
,As个数为![]() ,O和F的个数之和为2,F-的比例为x,O2-的比例为1-x,故该化合物的化学式为 SmFeAsO1-xFx ,1个晶胞的质量为
,O和F的个数之和为2,F-的比例为x,O2-的比例为1-x,故该化合物的化学式为 SmFeAsO1-xFx ,1个晶胞的质量为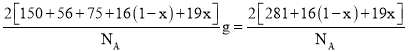 g,1个晶胞的体积为V=(a×10-10 pm)3= a3×10-30 cm3,则晶胞密度ρ=
g,1个晶胞的体积为V=(a×10-10 pm)3= a3×10-30 cm3,则晶胞密度ρ=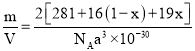 g/cm3;原子2位于底面面心,其坐标为(
g/cm3;原子2位于底面面心,其坐标为(![]() ,
,![]() ,0);原子3位于棱上,其坐标为(0,0,
,0);原子3位于棱上,其坐标为(0,0,![]() )。
)。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】优良的有机溶剂对孟烷、耐热型特种高分子功能材料![]() 的合成路线如图所示:
的合成路线如图所示:
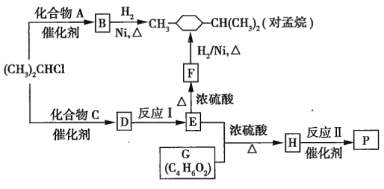
已知芳香化合物苯环上的氢原子可被卤代烷中的烷基取代,如:![]() (
(![]() 为烷基,
为烷基,![]() 为卤素原子)。
为卤素原子)。
(1)已知B为芳香烃。
①由B生成对孟烷的反应类型是__________________。
②![]() 与A反应生成B的化学方程式是_________________。
与A反应生成B的化学方程式是_________________。
③![]() 的同系物中相对分子质量最小的物质是_________________________。
的同系物中相对分子质量最小的物质是_________________________。
(2)已知![]() 的分子式为
的分子式为![]() 且含有一个酚羟基,且苯环上的另一个取代基与酚羟基处于间位;
且含有一个酚羟基,且苯环上的另一个取代基与酚羟基处于间位;![]() 不能使
不能使![]() 的
的![]() 溶液褪色。
溶液褪色。
①F中含有的官能团名称是_____________________。
②C的结构简式是________________。
③反应I的化学方程式是________________。
(3)G的核磁共振氢谱有3个峰,其峰面积之比为![]() ,且G与
,且G与![]() 溶液反应放出
溶液反应放出![]() 。写出反应Ⅱ的化学方程式:_________________________________。
。写出反应Ⅱ的化学方程式:_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“低碳经济”已成为全世界科学家研究的重要课题。为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究。
(1)已知:①CO(g)+H2O(g)![]() H2(g)+CO2(g) ΔH=-41 kJ·mol-1
H2(g)+CO2(g) ΔH=-41 kJ·mol-1
②C(s)+2H2(g) ![]() CH4(g) ΔH=-73 kJ·mol-1
CH4(g) ΔH=-73 kJ·mol-1
③2CO(g) ![]() C(s)+CO2(g) ΔH=-171 kJ·mol-1
C(s)+CO2(g) ΔH=-171 kJ·mol-1
写出CO2与H2反应生成CH4和H2O(g)的热化学方程式:____
(2)目前工业上有一种方法是用CO2来生产燃料甲醇。为探究该反应原理,在容积为2 L密闭容器中,充入1 mol CO2和3.25 mol H2在一定条件下发生反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间的变化如图所示:
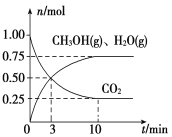
①从反应开始到平衡,氢气的平均反应速率v(H2)=________。
②下列措施一定不能使CO2的平衡转化率增大的是________。
A 在原容器中再充入1 mol CO2
B 在原容器中再充入1 mol H2
C 在原容器中充入1 mol氦气
D 使用更有效的催化剂
E 缩小容器的容积
F 将水蒸气从体系中分离
(3)煤化工通常研究不同条件下CO转化率以解决实际问题。已知在催化剂存在条件下反应:CO(g)+H2O(g) ![]() H2(g)+CO2(g)中CO的平衡转化率随p(H2O)/p(CO)及温度变化关系如图所示:
H2(g)+CO2(g)中CO的平衡转化率随p(H2O)/p(CO)及温度变化关系如图所示:

①上述反应的正反应方向是________反应(填“吸热”或“放热”);
②对于气相反应,用某组分(B)的平衡压强(pB)代替物质的量浓度(cB)也可以表示平衡常数(记作Kp),则该反应的Kp=_____(填表达式,不必代数计算);如果提高p(H2O)/p(CO),则Kp_______(填“变大”“变小”或“不变”)。使用铁镁催化剂的实际工业流程中,一般采用400 ℃左右、p(H2O)/p(CO)=3~5,采用此条件的原因可能是_______
(4)科学家用氮化镓材料与铜组装成如图所示的人工光合系统,利用该装置实现了用CO2和H2O合成CH4。下列关于该电池的叙述错误的是________。

A.该装置能量转化形式仅存在将太阳能转化为电能
B.铜电极为正极,电极反应式为CO2+8e-+8H+===CH4+2H2O
C.电池内部H+透过质子交换膜从左向右移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食品加工中常用焦亚硫酸钠(Na2S2O5)作漂白剂、防腐剂和疏松剂。现实验室欲制备焦亚硫酸钠,其反应依次为:(ⅰ)2NaOH+SO2=Na2SO3+H2O;
(ⅱ)Na2SO3+H2O+SO2=2NaHSO3;
(ⅲ)2NaHSO3![]() Na2S2O5+H2O。
Na2S2O5+H2O。
查阅资料:焦亚硫酸钠为黄色结晶粉末,150℃时开始分解,在水溶液或含有结晶水时更易被空气氧化。
实验装置如下:
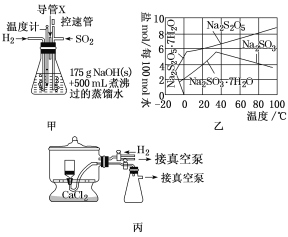
(1)实验室可用废铝丝与NaOH溶液制取H2,其离子方程式为___。
(2)通氢气一段时间后,以恒定速率通入SO2,开始的一段时间溶液温度迅速升高,随后温度缓慢变化,溶液开始逐渐变黄。“温度迅速升高”的原因为__。实验后期须利用水浴使温度保持在约80℃。
(3)反应后的体系中有少量白色亚硫酸钠析出,除去其中亚硫酸钠固体的方法是___;然后获得较纯的无水Na2S2O5,应将溶液冷却到30℃左右过滤,控制“30℃左右”的理由是___。
(4)丙为真空干燥Na2S2O5晶体的装置,通入H2的目的是___。
(5)常用剩余碘量法测定产品中焦亚硫酸钠的质量分数。已知:S2O52-+2I2+3H2O=2SO42-+4I-+6H+;2S2O32-+I2=S4O62-+2I-。请补充实验步骤(可提供的试剂有:焦亚硫酸钠样品、标准碘溶液、淀粉溶液、酚酞溶液、标准Na2S2O3溶液及蒸馏水)。
①精确称取产品0.2000g放入碘量瓶(带磨口塞的锥形瓶)中。
②准确移取一定体积的已知浓度的标准碘溶液(过量)并记录数据,在暗处放置5min,然后加入5mL冰醋酸及适量的蒸馏水。
③用标准Na2S2O3溶液滴定至接近终点。
④___。
⑤重复步骤①~③;根据相关记录数据计算出平均值。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚苯乙烯的结构简式为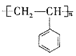 ,试回答下列问题:
,试回答下列问题:
(1)聚苯乙烯的分子式为__________,链节是____________,单体是_________________。
(2)实验测得聚苯乙烯的相对分子质量(平均值)为52000,则该高聚物的聚合度![]() 为________。
为________。
(3)一定条件下合成聚苯乙烯的化学方程式为______,该反应类型为_______反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)单质铜及镍都是由________键形成的晶体;元素铜与镍的第二电离能分别为:ICu=1958 kJ/mol、INi=1753 kJ/mol,ICu>INi的原因是_____________________。
(2)某镍白铜合金的立方晶胞结构如图所示。
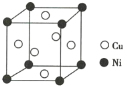
①晶胞中铜原子与镍原子的数量比为________。
②合金的密度为d g/cm3,晶胞参数a=________nm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物X、Y、M(已知M为乙酸)的转化关系为:淀粉→X→Y![]() 乙酸乙酯,下列说法错误的是
乙酸乙酯,下列说法错误的是
A.X可用新制的氢氧化铜悬浊液检验
B.实验室由Y和M制取乙酸乙酯时可用饱和NaOH溶液来提纯
C.由Y生成乙酸乙酯的反应属于取代反应
D.可用碘水检验淀粉是否水解完全
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若在一定条件下,容积恒定的反应室中充入amolCO与2amolH2,在催化剂作用下发生反应CO(g)+2H2(g)![]() CH3OH(g),下列措施一定使
CH3OH(g),下列措施一定使![]() 增大的是( )
增大的是( )
A.升高温度B.充入Ar(g)使体系的总压增大
C.恒温恒容再充入H2D.恒温恒容再充入amolCO和2amolH2
查看答案和解析>>
科目:高中化学 来源: 题型:
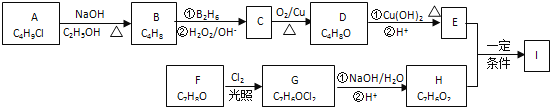
【题目】化合物Ⅰ(C11H12O3)是制备液晶材料的中间体之一,其分子中含有醛基和酯基.
Ⅰ可以用E 和H在一定条件下合成:
已知:①A的核磁共振氢谱表明其只有一种化学环境的氢;
②RCH=CH2![]() RCH2CH2OH
RCH2CH2OH
③化合物F苯环上的一氯代物只有两种;
④通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基
(1)A的化学名称为_____________;
(2)D的结构简式为_____________;
(3)I的结构简式为_____________;
(4)写出下列反应的类型:A→B:____________;C→D:____________;
(5)F生成G的化学方程式为:______________;
(6)I的同系物J比I相对分子质量小14,J能同时满足如下条件:①苯环上只有两个取代基,②能发生银镜反应,③能和饱和NaHCO3溶液反应放出CO2;符合上述条件的同分异构体共有__________种(不考虑立体异构).若J的一个同分异构体发生银镜反应并酸化后核磁共振氢谱为三组峰,且峰面积比为2:2:1,写出J的这种同分异构体的结构简式___________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com