


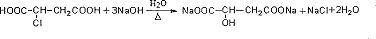
 等.
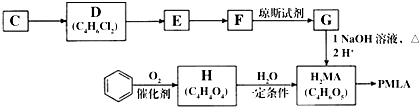
等. 分析 1 mol有机物H与足量NaHC03溶液反应生成标准状况下的C02 44.8L,二氧化碳为2mol,说明H分子中有2个羧基,H有顺反异构,所以H中还有碳碳双键,则H为HOOC-CH=CH-COOH,由H、H2MA的分子式可知,H与水发生加成反应生成H2MA为 ,H2MA发生缩聚反应得到PMLA为
,H2MA发生缩聚反应得到PMLA为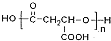 等,从G到H2MA发生水解、酸化,故G为
等,从G到H2MA发生水解、酸化,故G为 ,由D到G中官能团的变化可知,D为ClCH2CH=CHCH2Cl,D在氢氧化钠水溶液、加热条件下发生水解反应生成E为
,由D到G中官能团的变化可知,D为ClCH2CH=CHCH2Cl,D在氢氧化钠水溶液、加热条件下发生水解反应生成E为 ,E与HCl发生加成反应生成F为
,E与HCl发生加成反应生成F为 ,F与琼斯试剂反应得到G,据此解答.
,F与琼斯试剂反应得到G,据此解答.
解答 解:1 mol有机物H与足量NaHC03溶液反应生成标准状况下的C02 44.8L,二氧化碳为2mol,说明H分子中有2个羧基,H有顺反异构,所以H中还有碳碳双键,则H为HOOC-CH=CH-COOH,由H、H2MA的分子式可知,H与水发生加成反应生成H2MA为 ,H2MA发生缩聚反应得到PMLA为
,H2MA发生缩聚反应得到PMLA为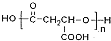 等,从G到H2MA发生水解、酸化,故G为
等,从G到H2MA发生水解、酸化,故G为 ,由D到G中官能团的变化可知,D为ClCH2CH=CHCH2Cl,D在氢氧化钠水溶液、加热条件下发生水解反应生成E为
,由D到G中官能团的变化可知,D为ClCH2CH=CHCH2Cl,D在氢氧化钠水溶液、加热条件下发生水解反应生成E为 ,E与HCl发生加成反应生成F为
,E与HCl发生加成反应生成F为 ,F与琼斯试剂反应得到G,
,F与琼斯试剂反应得到G,
(1)H为HOOC-CH=CH-COOH,其反式结构简式是 ,故答案为:
,故答案为: ;
;
(2)由上述分析可知,E的结构简式为 ,故答案为:
,故答案为: ;
;
(3)G中羧基、氯原子均与氢氧化钠发生反应,G与氢氧化钠溶液的反应化学方程式为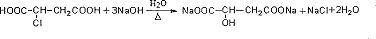 ,
,
故答案为: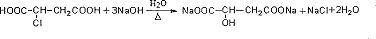 ;
;
(4)H为HOOC-CH=CH-COOH,为对称分子,羧基和-CH=中各有1种H原子,所以共2个吸收峰,
故答案为:2;
(5)由H2MA制PMLA发生脱水缩合反应,化学方程式为: 等,
等,
故答案为: 等.
等.
点评 本题考查有机物的推断与合成,注意根据H的分子式与生成二氧化碳确定H的结构是关键,结合分子式推断H2MA的结构,再结合D到G中官能团的变化综合分析推断,侧重考查学生分析推理能力,难度中等.


科目:高中化学 来源: 题型:多选题
| A. | 测定中和热时,大小两烧杯间填满碎纸的作用只是固定小烧杯 | |
| B. | 用50mL 0.50mo1•L-1的氢氧化钠溶液,分别与50mL 0.50mo1•L-1的盐酸和50mL 0.25mo1•L-1的硫酸充分反应,两反应测定的中和热相等 | |
| C. | 不能用铜丝代替玻璃棒搅拌酸碱混合液 | |
| D. | 酸碱混合时,量筒中NaOH溶液应缓缓倒入小烧杯中,不断用玻璃棒搅拌 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间(s) | 0 | 10 | 20 | 25 | 30 |
| 条件A[n(NO2)](mol) | 0.20 | 0.14 | 0.13 | 0.13 | 0.13 |
| 条件B[n(NO2)](mol) | 0.20 | 0.10 | 0.10 | 0.10 | 0.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某化学兴趣小组为了探究某些气体的性质,设计了如图所示的实验装置.实验时将A、D中产生的气体同时通入C中.(K为止水夹,部分夹持仪器已略去)
某化学兴趣小组为了探究某些气体的性质,设计了如图所示的实验装置.实验时将A、D中产生的气体同时通入C中.(K为止水夹,部分夹持仪器已略去)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca2+:1s22s22p63s23p6 | B. | O:1s22s22p6 | ||
| C. | P:1s22s22p63s23p3 | D. | Br:1s22s22p63s23p63d104s24p5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com