
【题目】下列物质转化需要加入还原剂才能实现的是
A. SO32-→SO2B. HCl→Cl2C. Na→Na+D. SO2→S
科目:高中化学 来源: 题型:
【题目】下列各组数据中,前者刚好是后者两倍的是 ( )
A. 2 mol H2O的摩尔质量和1 mol H2O的摩尔质量
B. 200 mL 1 mol·L-1氯化钙溶液中c(Cl-)和100 mL 2 mol·L-1氯化钾溶液中c(Cl-)
C. 64 g二氧化硫中氧原子数和标准状况下22.4 L一氧化碳中氧原子数
D. 20% NaOH溶液中NaOH的物质的量浓度和10% NaOH溶液中NaOH的物质的量浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某三原子分子构成的气体,其摩尔质量为M g/mol,该气体质量为m g,阿伏加德罗常数为NA , 则:
(1)该气体在标准状况下的体积为 ________ L.
(2)该气体在标准状况下的密度为 ________ g/L.
(3)该气体所含原子总数为 ________ 个.
(4)该气体的一个分子的质量为 ________ g.
(5)该气体完全溶于水形成V L溶液(不考虑反应),所得溶液的物质的量浓度为________mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】尽管氮元素在地壳中的含量较低(主要以硝酸盐的形式存在),但是大气中有丰富的氮气,这为氨和硝酸的广泛应用提供了可能。
(1)氮气的电子式为________,雷电作用能进行氮的固定,写出反应方程式________。
(2)食物蕴含的营养物质中,含氮的高分子化合物是_____(填名称,下同),其水解的最终产物为________。
(3)土壤中的NH4+在硝化细菌的催化作用下可被氧化成NO3﹣,写出其离子方程式:________。
(4)某镁铝合金用足量稀硝酸完全溶解,得到标准状况下NO 11.2L,再向溶液中加入过量氨水,充分反应后过滤.若沉淀质量为40.8g,则合金的质量为________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的氯气通入30 mL浓度为10 mol/L的氢氧化钠浓溶液中,加热少许时间后均完全反应溶液中形成NaCl、NaClO、NaClO3共存体系。下列判断正确的是( )
A. Cl2在反应中仅作氧化剂
B. ClO3—中心原子采用sp2杂化
C. n(NaCl)∶n(NaClO)∶n(NaClO3)可能为11∶2∶1
D. 与NaOH反应的氯气一定为0.15 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用CO和H2反应制备二甲醚(CH3OCH3)的条件是压力2.0~10.0MPa,温度300℃。设备中进行下列反应,请回答下列问题:
①CO(g)+2H2(B)![]() CH3OH(g) △H=-90.7kJ/mol
CH3OH(g) △H=-90.7kJ/mol
②2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H=-23.5kJ/mol
CH3OCH3(g)+H2O(g) △H=-23.5kJ/mol
③CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=-41.2kJ/mol
CO2(g)+H2(g) △H=-41.2kJ/mol
(1)总反应3CO(g)+3H2(g)=CH3OCH3(g)+CO2(g)的△H=_____________ 。据此可判断该反应_________________条件下自发。
(2)在温度和容积不变的条件下发生反应①,能说明该反应达到平衡状态的依据是_____
a.容器中压强保持不变 b.混合气体中c(CO)不变
c.v正(CO)= v逆(H2) d.c(CH3OH)= c(CO)
(3)在2L 的容器中加入amol CH3OH(g)发生反应②,达到平衡后若再加入amolCH3OH(g)重新达到平衡时,CH3OH 的转化率____________(填“增大”、“ 减小”或“不变”)。
(4)850℃时在一体积为10L 的容器中通入一定量的CO和H2O(g)发生反应③,CO和H2O(g)浓度变化如图所示。
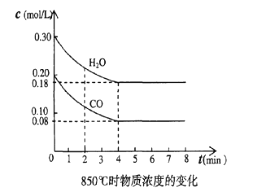
①0~4min 的平均反应速率,v(CO)=________________ 。
②若温度不变,向该容器中加入4mo1CO(g)、2mo1H2O(g)、3mo1CO2(g)和3molH2(g),起始时v正(CO)______v逆(H2)(填“<”、“ >”或“=”),请结合必要的计算说明理由。________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com