
【题目】为了研究碳酸钙与稀盐酸反应的反应速率,某同学通过实验测定反应中生成的CO2气体体积随反应时间变化的情况(0~t1、t1~t2 、t2~t3各时间段相同),绘制出如图所示的曲线。下列说法不正确的是

A.反应速率最大的是0~t1段,生成气体最多的是t3~t4段
B.t1~t2段曲线变化的可能是盐酸与大理石反应放热导致的
C.t2~t3时间段里影响反应速率的主要外界因素是浓度
D.为了减缓反应速率可向盐酸中加入NaCl溶液
科目:高中化学 来源: 题型:
【题目】在密闭系统中有反应C(s)+CO2(g)![]() 2CO(g),能使反应速率加快的措施是
2CO(g),能使反应速率加快的措施是
①通过减小容器体积增大压强 ②升高温度③将炭粉碎 ④通入CO2 ⑤增加炭的量 ⑥恒容条件下通入N2
A.①②③④B.①②④⑥C.①②③⑥D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以芳香烃A(苯环上只有一个侧链)为原料发生如图所示的变化,可以合成高聚物G。

已知:①两个羟基连在同一碳原子上不稳定,会自动脱水。如: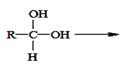 R—CHO
R—CHO
②C能发生银镜反应,F能使溴水褪色。
回答下列问题:
(1)A中官能团的名称是___;C的结构简式为___。
(2)B→C的反应条件是___,E→F的反应类型是___。
(3)写出E→G的化学方程式___。
(4)E的同分异构体中,苯环上有3个取代基、遇FeCl3溶液显紫色且能与碳酸氢钠溶液反应的共有___种(不考虑立体异构)。
(5)参照上述合成路线,设计以丙炔为原料制备乳酸(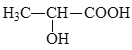 )的合成路线___(无机试剂任选)。
)的合成路线___(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D为由短周期元素组成的四种物质,它们有如下所示转化关系,且D为强电解质(其他相关物质可能省略)。

下列说法不正确的是
A. 若A为非金属单质,则它与Mg反应的产物中阴、阳离子个数比可能为2:3
B. 若A为非金属单质,则其组成元素在周期表中的位置可能处于第二周期第IVA族
C. 若A是共价化合物,则A和D有可能发生氧化还原反应
D. 若A是金属或非金属单质,则常温下0. 1 mol/L的D溶液中由水电离出的c(H+)可能为10-13mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某课外小组设计的实验室制取乙酸乙酯的装置如下图所示。请回答:
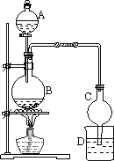
①若用 18O 标记乙醇中的氧原子,则 CH3CH218OH 与乙酸反应的化学方程式是_____________。
②球形干燥管C 的作用是______________。
③D 中选用饱和碳酸钠溶液的原因是_____________。
④反应结束后D 中的现象是_____________。
⑤下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有_____________(填序号)。
A.单位时间里,生成 1mol 乙酸乙酯,同时生成 1mol 水
B.单位时间里,消耗 1mol 乙醇,同时消耗 1mol 乙酸
C.正反应的速率与逆反应的速率相等
D.混合物中各物质的浓度不再变化
(2)N-苯基苯甲酰胺( 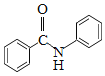 )广泛应用于药物,可由苯甲酸(
)广泛应用于药物,可由苯甲酸(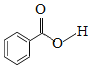 )与苯胺(
)与苯胺(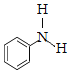 )反应制得,由于原料活性低,可采用硅胶催化、微波加热的方式,微波直接作用于分子,促进活性部位断裂,可降低反应温度。取得粗产品后经过洗涤—重结晶等,最终得到精制的成品。
)反应制得,由于原料活性低,可采用硅胶催化、微波加热的方式,微波直接作用于分子,促进活性部位断裂,可降低反应温度。取得粗产品后经过洗涤—重结晶等,最终得到精制的成品。
已知:
| 水 | 乙醇 | 乙醚 |
苯甲酸 | 微溶 | 易溶 | 易溶 |
苯胺 | 易溶 | 易溶 | 易溶 |
N-苯基苯甲酰胺 | 不溶 | 易溶于热乙醇,冷却后易 于结晶析出 | 微溶 |
下列说法不正确的是_____________(填字母编号)。
A.反应时断键位置为C—O 键和 N—H 键
B.洗涤粗产品用水比用乙醚效果更好
C.产物可选用乙醇作为溶剂进行重结晶提纯
D.硅胶吸水,能使反应进行更完全
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,当Mg(OH)2固体在水溶液中达到下列平衡时:Mg(OH)2(s)![]() Mg2+(aq)+2OH-(aq),若使固体Mg(OH)2的量减少,而且c(Mg2+)不变,可采取的措施是:
Mg2+(aq)+2OH-(aq),若使固体Mg(OH)2的量减少,而且c(Mg2+)不变,可采取的措施是:
A. 加MgCl2B. 加H2OC. 加NaOHD. 加HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,在浓度为1mol/L的(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2的溶液中,测其c(NH4+)分别为a、b、c(单位为mol/L),下列判断正确的是
A. a=b=c B. a>b>c C. a>c>b D. c>a>b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜铟镓硒薄膜太阳能电池(GIGS)是第三代太阳能电池的典型代表,已成为全球光伏领域研究的热点之一,回答下列问题:
(1)镓(Ga)价电子排布式为______,镓(Ga)与铟(In)同主族第一电离能较小的为______(用元素符号表示)。
(2)硒属于_______区元素。O、S、Se简单氢化物稳定性由強到弱的顺序为______,中心原子的杂化方式为___________,键角最大的是_____________。
(3)已知N-N、N=N键能之比为l:4.9,而C-C、C=C键能之比为1:2.34。则N2和C2H2中叁键能较大的是__________ (填化学式)。
(4)某晶体的晶胞结构如图所示(在该晶体中通过掺入适量的Ga以替代部分In就可以形GIGS晶体),该晶体的化学式为__________。

图中A原子和B原子坐标(分别为(0,0,0),(0,0, ![]() ),则C原子坐标为_________。
),则C原子坐标为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.10 mol镁条在只含有CO2和O2混合气体的容器中燃烧(产物不含碳酸镁),反应后容器内固体物质的质量不可能为( )
A. 3.2 g B. 4.0 g C. 4.2 g D. 4.6 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com