
【题目】用酸性甲醛燃料电池为电源进行电解的实验装置如图所示,下列说法中正确的是

A. 当a、b都是铜作电极时,电解的总反应方程式为2CuSO4+2H2O![]() 2H2SO4+2Cu+O2↑
2H2SO4+2Cu+O2↑
B. 燃料电池工作时,正极反应为O2+2H2O+4e-===4OH-
C. 当燃料电池消耗22.4 L甲醛气体时,电路中理论上转移2 mol e-
D. 燃料电池工作时,负极反应为HCHO+H2O-2e-===HCOOH+2H+
【答案】D
【解析】
左边装置是酸性甲醛燃料电池,原电池放电时,燃料失去电子发生氧化反应,所以通入燃料的电极为负极,通入氧气的电极为正极,正极上氧化剂得到电子发生还原反应,由于电解质溶液呈酸性,正极上电极反应为O2+4H++4e-=2H2O,右边装置有外界电源,所以是电解池,连接负极的a电极时阴极,连接正极的b极是阳极,阳极上失去电子发生氧化反应,阴极上得到电子发生还原反应。
A. 当a、b都是铜作电极时,形成电解精炼装置,阳极铜失去电子,阴极上铜离子得到电子,故错误;B.由于电解质溶液呈酸性,正极反应为O2+4H++4e-=2H2O ,故错误;C. 当燃料电池消耗22.4 L甲醛气体时,由于没有说明是在标况下,所以无法计算甲醛的物质的量,则无法计算转移电子的物质的量,故错误;D. 燃料电池工作时,甲醛在负极上失去电子生成甲酸,则负极反应为HCHO+H2O-2e-=HCOOH+2H+,故正确。故选D。


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:
【题目】【加试题】甲醇水蒸气重整制氢(SRM)是用于驱动电动汽车的质子交换膜燃料电池的理想氢源,当 前研究主要集中在提高催化剂活性和降低尾气中CO含量,以免使燃料电池Pt电极中毒。重整过程发生的反应如下:
反应I CH3OH(g)+H2O(g) ![]() CO2(g)+3H2(g) ΔH1
CO2(g)+3H2(g) ΔH1
反应Ⅱ CH3OH(g) ![]() CO(g)+2H2(g) ΔH2
CO(g)+2H2(g) ΔH2
反应Ⅲ.CO(g)+H2O(g) ![]() CO2(g)+H2(g) ΔH3
CO2(g)+H2(g) ΔH3
其对应的平衡常数分别为K1、K2、K3,其中K2、K3随温度变化如下表所示:
125℃ | 225℃ | 325℃ | |
K2 | 0.5535 | 185.8 | 9939.5 |
K3 | 1577 | 137.5 | 28.14 |
请回答:
(1)反应Ⅱ能够自发进行的条件_______ (填 “低温”、“高温”或“任何温度”), ΔH1____ΔH3 (填 “>”、“<”或 “=” )。
(2)相同条件下,甲醇水蒸气重整制氢较甲醇直接分解制氢(反应Ⅱ)的先进之处在于_________。
(3)在常压、CaO催化下,CH3OH和H2O混和气体(体积比1∶1.2,总物质的量2.2mol)进行反应,tl时刻测得 CH3OH转化率及CO、CO2选择性随温度变化情况分别如图所示(CO、CO2的选择性:转化的CH3OH中生成CO、CO2的百分比)。
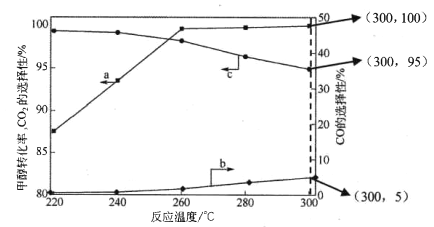
注:曲线a表示CH3OH的转化率,曲线b表示CO的选择性,曲线c表示 CO2的选择性
① 下列说法不正确的是_____。
A.反应适宜温度为300℃
B.工业生产通 常在负压条件下进行甲醇水蒸气重整
C.己知 CaO催化剂具有更高催化活性,可提高甲醇平衡转化率
D.添加CaO的复合催化剂可提高氢气产率
② 260℃ 时H2物质的量随时间的变化曲线如图所示。画出300℃时至t1时刻H2物质的量随时间的变化曲线_____。
(4)副产物CO2可以在酸性水溶液中电解生成甲酸,生成甲酸的电极反应式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在火箭推进器中装有还原剂肼(N2H4)和强氧化剂H2O2,当它们混合时,即产生大量的的氮气和水蒸气,并放出大量的热量.已知0.4mol液态肼和足量双氧水反应生成氮气和水蒸气时放出256.65KJ的热量。
(1)写出肼和过氧化氢的结构式肼_______,过氧化氢_________。
(2)上述反应应用于火箭推进剂,除释放出大量热量和快速产生大量气体外,还有一个很突出的优点是______。
(3)写出肼和双氧水反应的热化学方程式___________。
(4)已知H2O(l)═H2O(g);△H=+44KJ/mol,则16g液态肼与足量双氧水反应生成氮气和液态水时,放出的热量是_________。
(5)已知:
N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-543kJ/mol
则肼与NO2完全反应的热化学方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机化合物A的结构简式如下:

(1)A的分子式是________。
(2)A在NaOH溶液中充分加热后,再加入过量的盐酸酸化后,可得到B、C、D和![]() 四种有机物,且相对分子质量大小关系为B>C>D,则B、C、D的结构简式分别是B________;C________;D________。
四种有机物,且相对分子质量大小关系为B>C>D,则B、C、D的结构简式分别是B________;C________;D________。
(3)在B的同分异构体中,属于1,3,5三取代苯的化合物的结构简式__________________。
(4)写出B与碳酸氢钠反应的化学方程式:________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示气体体积均在相同状况下测定)。欲使溶液恢复到起始状态,可向溶液中加入

A. 0.1 mol CuO
B. 0.1 mol CuCO3
C. 0.05 mol Cu2(OH)2CO3
D. 0.1 mol Cu(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2﹣氨基﹣3﹣氯苯甲酸(H)是重要的医药中间体,可以用来合成许多重要有机物,其制备流程图如下:

已知: 
回答下列问题:
(1)反应①的反应类型是________。
(2)写出反应②的化学反应方程式________。
(3)该流程未采用甲苯直接硝化的方法制备B,而是经由①②③三步反应制取B,目的是__________。
(4)E的结构简式为_______,对比D与H的结构简式,设计⑥~⑨四步反应实现转化的目的是_______。
(5)写出⑧的反应试剂和条件:_____。
(6)J是一种高分子化合物,写出反应⑩的化学反应方程式:_____。
(7)写出符合下列条件的B的所有同分异构体的结构简式__________。
a.苯环上只有两个取代基且互为邻位
b.既能发生银镜反应又能发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式中,不正确的是( )
A.HCl═H++Cl﹣
B.NH3H2O═NH4++OH﹣
C.CaCl2=Ca2++2Cl﹣
D.CH3COOHCH3COO﹣+H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种重要的化工原料,又是一种可再生能源,具有开发和应用的广阔前景。
(1)已知:CH3OH(g)===HCHO(g)+H2(g) ΔH=+84 kJ·mol-1
2H2(g)+O2(g)===2H2O(g) ΔH=-484 kJ·mol-1
①工业上常以甲醇为原料制取甲醛,请写出CH3OH(g)与O2(g)反应生成HCHO(g)和H2O(g)的热化学方程式:______________________________________________。
②在上述制备甲醛时,常向反应器中通入适当过量的氧气,其目的_________________。
(2)工业上可用如下方法合成甲醇,化学方程式为CO(g)+2H2(g)==CH3OH(g),已知某些化学键的键能数据如下表:
化学键 | C—C | C—H | H—H | C—O | C≡O | O—H |
键能/(kJ·mol-1) | 348 | 413 | 436 | 358 | x | 463 |
请回答下列问题:
①图1中曲线a到曲线b的措施是_________。

②已知CO中的C与O之间为叁键,其键能为x kJ/mol,则x=________。
(3)由甲醇、氧气和NaOH溶液构成的新型手机电池,可使手机连续使用一个月才充一次电。
①该电池负极的电极反应式为______________________________________。
②若以该电池为电源,用石墨作电极电解200 mL含有如下离子的溶液。
离子 | Cu2+ | H+ | Cl- | SO42- |
c/(mol·L-1) | 0.5 | 2 | 2 | 0.5 |
电解一段时间后,当两极收集到相同体积(相同条件下)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象)阳极上收集到氧气的质量为________。
(4)电解水蒸气和CO2产生合成气(H2
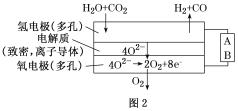
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究影响化学反应速率的因素:在25mL 5%的H2O2溶液中,如表格中条件,产生等体积氧气时,所消耗时间最短的是:
组别 | V(1mol/L FeCl3)/mL | 蒸馏水/mL | 温度/℃ |
A | 2 | 2 | 50 |
B | 3 | 1 | 40 |
C | 2 | 2 | 40 |
D | 3 | 1 | 50 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com