
【题目】在容积为2L的密闭容器中充入3mol气体A和2.5mol气体B,发生反应:3A(g)+B(g)xC(g)+2D(g)(正反应为吸热反应),5min时测得生成1mol D,C的平均反应速率v(C)=0.1molL﹣1min﹣1 , 试求:
(1)方程式中C的化学计量数x= .
(2)5min内A的平均反应速率v(A)= .
(3)5min时B的转化率为 .
(4)温度升高A的转化率(填“增大”或“减小”或“不变”下同),压强增大B的转化率 .
【答案】
(1)2
(2)0.15mol/L?min
(3)20%
(4)增大;不变
【解析】解:C的平均反应速率v(C)=0.1molL﹣1min﹣1 , 反应生成C物质的量=0.1molL﹣1min﹣1×2L×5min=1mol;
3A(g)+ | B(g) | xC(g)+ | 2D(g) | ||
起始量(mol): | 3 | 2.5 | 0 | 0 | |
变化量(mol): | 1.5 | 0.5 | 0.5x | 1 | |
平衡量(mol): | 1.5 | 2 | 0.5x | 1 |
1)上述计算结合反应生成的C物质的量计算得到x,0.5x=1,x=2;
故答案为:2;(2)5min内A的平均反应速率= ![]() =
= ![]() =0.15mol/Lmin;
=0.15mol/Lmin;
故答案为:0.15mol/Lmin;(3)5min时B的转化率= ![]() ×100%=
×100%= ![]() ×100%=20%;
×100%=20%;
故答案为:20%;(4)由题意可知,正反应为吸热反应,所以升高温度,平衡向正反应方向移动,所以A的转化率增大,由(1)计算得x=2,所以该反应为气体体积不变的反应,增大压强,平衡不移动,所以B的转化率不变,
故答案为:增大;不变.
结合化学平衡三段式列式计算,C的平均反应速率v(C)=0.1molL﹣1min﹣1 , 反应生成C物质的量=0.1molL﹣1min﹣1×2L×5min=1mol;
3A(g)+ | B(g) | xC(g)+ | 2D(g) | ||
起始量(mol): | 3 | 2.5 | 0 | 0 | |
变化量(mol): | 1.5 | 0.5 | 0.5x | 1 | |
平衡量(mol): | 1.5 | 2 | 0.5x | 1 |
1)依据上述计算结合反应生成的C物质的量计算得到x;(2)反应速率= ![]() ;(3)转化率=
;(3)转化率= ![]() ×100%;(4)由题意可知,正反应为吸热反应,所以升高温度,平衡向正反应方向移动,由(1)计算得x,根据增大压强,平衡向气体体积减小的方向移动进行判断.
×100%;(4)由题意可知,正反应为吸热反应,所以升高温度,平衡向正反应方向移动,由(1)计算得x,根据增大压强,平衡向气体体积减小的方向移动进行判断.


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 镍氢电池、锂电池和碱性锌锰干电池都是二次电池
B. 氢氧燃料电池是一种高效且不会污染环境的新型电池
C. 铅蓄电池放电的时候正极材料是铅,负极材料是二氧化铅
D. 铅蓄电池充电时将化学能转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于自然界中氮循环示意图(如图)的说法错误的是( ) 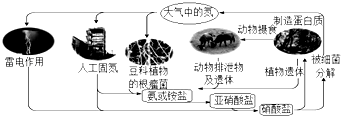
A.氮元素只被氧化
B.豆科植物根瘤菌固氮属于自然固氮
C.其它元素也参与了氮循环
D.含氮无机物和含氮有机物可相互转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列制取蒸馏水的实验装置与操作的说法中,不正确的是( )
A. 温度计的水银球应插入蒸馏烧瓶中的自来水中
B. 冷凝管中的水流方向是从下口进入,上口排出
C. 实验中需要在蒸馏烧瓶中加入几粒碎瓷片,防止出现暴沸现象
D. 加热蒸馏烧瓶必须垫石棉网
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法不正确的是
A. 苯中碳碳键是介于C-C和C=C之间的一种特殊共价键
B. 甲烷、乙烯都能使酸性KMnO4溶液褪色
C. 葡萄糖溶液中加入银氨溶液,水浴加热有银镜生成
D. 医用酒精能使蛋白质变性,可用于消毒杀菌
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为落实“五水共治”,某工厂拟综合处理含NH4+废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如图流程: 
(1)固体I中主要成分为 , 捕获剂所捕获的气体主要是 .
(2)处理含NH4+废水时,发生反应的离子方程式为 .
(3)若X为适量空气,严格控制空气用量的原因是 .
(4)工业废气中的SO2、NO还可采用NaClO2溶液作为吸收剂进行净化,在鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323K,NaClO2溶液浓度为5×10﹣3molL﹣1 . 反应一段时间后溶液中离子浓度的分析结果如表:
离子 | SO42﹣ | SO32﹣ | NO3﹣ | NO2﹣ | Cl﹣ |
c(molL﹣1) | 8.35×10﹣4 | 6.87×10﹣6 | 1.5×10﹣4 | 1.2×10﹣5 | 3.4×10﹣3 |
①写出NaClO2溶液脱硝过程中主要反应的离子方程式 .
增加压强,NO的转化率(填“提高”、“不变”或“降低”).
②随着吸收反应的进行,吸收剂溶液的pH逐渐(填“增大”、“不变”或“减小”).
③如果采用NaClO、Ca(ClO)2替代NaClO2 , 也能得到较好的烟气脱硫效果.从化学平衡原理分析,Ca(ClO)2相比NaClO具有的优点是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中都正确的选项是( )
①用剩后的药品为避免浪费应放回原瓶
②蒸发氯化钠溶液时要用玻璃棒不断搅动
③称取易潮解的药品时必须放在玻璃器皿中称量
④浓硫酸沾到皮肤上,立即用大量水冲洗,然后涂上NaOH溶液
A. ②③ B. ②③④ C. ②④ D. ①②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com