
 过氧乙酸是高效、速效、广谱灭菌剂.实验室合成与含量测定的相关步骤如下:
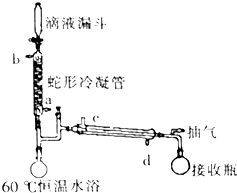
过氧乙酸是高效、速效、广谱灭菌剂.实验室合成与含量测定的相关步骤如下: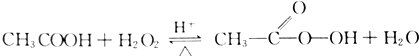 ,向装有搅拌装置及温度计的500ml三口烧瓶中先加入16.0g冰醋酸,然后在搅拌下滴加90g浓缩后的H2O2溶液,最后加入7.5ml浓硫酸,搅拌下加热5h,静置20h.
,向装有搅拌装置及温度计的500ml三口烧瓶中先加入16.0g冰醋酸,然后在搅拌下滴加90g浓缩后的H2O2溶液,最后加入7.5ml浓硫酸,搅拌下加热5h,静置20h.分析 (1)球形冷凝管的进水口为下进上出;
(2)增大反应物的浓度,平衡向正反应方向移动;浓硫酸除起到催化剂的作用之外,还起到吸水剂的作用,有利于反应向正方向进行,提高产率;
(3)充分搅拌,能使反应物充分接触,提高提高原料利用率;
(4)根据用2.0g过氧乙酸样品,配制成100mL溶液步骤选用仪器,然后判断还缺少仪器名称;
(5)过氧化氢和高锰酸钾在酸性条件下发生氧化还原反应,硫酸锰做催化剂作用;
(6)根据已知方程式列出关系式:CH3COOOH~I2~2S2O32-,根据关系式求解5mL溶液A中含CH3COOOH质量,据此计算原试样中过氧乙酸的质量分数.
解答 解:(1)球形冷凝管的进水应克服水的重力充满冷凝管口,方向为下进上出,即从a口进,
故答案为:a;
(2)合成过氧乙酸:CH3COOH+H2O2$\stackrel{H+}{?}$CH3COOOH+H2O,该反应为可逆反应,增大反应物的浓度,平衡向正反应方向移动,用68%的H2O2溶液代替30%的H2O2溶液,可增大反应速率,同时有利于平衡向生成过氧乙酸的方向移动,合成过氧乙酸:CH3COOH+H2O2$\stackrel{H+}{?}$CH3COOOH+H2O,该反应为可逆反应,为提高反应物的产率,加入浓硫酸除起到催化剂的作用之外,还起到吸水剂的作用,有利于反应向正方向进行,提高产率,
故答案为:增大过氧化氢的浓度,有利于平衡向生成过氧乙酸的方向移动;催化剂、吸水剂;
(3)充分搅拌,能使反应物充分接触,提高提高原料利用率,
故答案为:使反应物充分接触,提高原料利用率;
(4)配制100mL过氧乙酸溶液,配制步骤为:计算、称量(量取)、溶解、转移、洗涤、定容,称量时用到仪器是天平、药匙(量取时用到量筒),溶解时用到烧杯、玻璃棒,转移溶液时用到玻璃棒、容量瓶,定容时用到胶头滴管,其中属于玻璃仪器的是玻璃棒、烧杯、胶头滴管、量筒、容量瓶,故还需要的玻璃仪器有100mL容量瓶、胶头滴管,
故答案为:100mL容量瓶、胶头滴管;
(5)过氧化氢和高锰酸根离子发生氧化还原反应:MnO4-+H2O2+H+-Mn2++O2↑+H2O中,Mn的化合价从+7降低为+2价,降低了5价,O的化合价从-1价升高到了0价,两个氧原子一共升高了2价,所以Mn元素的前边系数是2,双氧水的前边系数是5,根据电荷守恒和原子守恒,得到反应为:2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O,硫酸锰做此反应的催化剂,
故答案为:催化剂;
(6)根据已知方程式CH3COOOH+2H++2I-═I2+CH3COOH+H2O①,I2+2S2O32-═2I-+S4O42-②,可得关系式:CH3COOOH~I2~2S2O32-,5mL溶液A中含CH3COOOH,
CH3COOOH~I2~2S2O32-,
1 2
n(CH3COOOH) 0.050mol•L-1×20×10-3L
n(CH3COOOH)=5×10-4mol,
称取2.0g过氧乙酸样品,配制成100mL溶液A,100mL溶液A,n(CH3COOOH)=5×10-4mol×$\frac{100ml}{5ml}$=1×10-2mol,原试样中过氧乙酸的质量分数为$\frac{1×1{0}^{-2}mol×78g/mol}{2g}$×100%=38%,
故答案为:38%.
点评 本题以过氧乙酸为载体考查溶液的浓缩、物质的合成、含量的测定等,侧重考查分析和计算能力,明确每一过程发生的反应是解本题关键,知道各种物质的性质,根据方程式进行计算即可,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题

 .
. .
. .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②的溶液变黄的原因是反应产生Fe3+ | |
| B. | 上述实验中,共有两个氧化还原反应 | |
| C. | 实验①生成的气体不能使湿润的淀粉KI试纸变蓝 | |
| D. | 实验②证明Fe2+既有氧化性又有还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 晶体硅是一种半导体材料,常用于制造光导纤维 | |
| B. | 发酵粉中含有碳酸氢钠,能使焙制出的糕点疏松多孔 | |
| C. | 铜能与氯化铁溶液反应,该反应可以应用于印刷电路板的制作 | |
| D. | 金属钠可用于冶炼钛等金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知同温同压下烃A的密度与N2相同,C可发生银镜反应.它们之间的转化关系如图(部分反应条件和产物略去).请回答:
已知同温同压下烃A的密度与N2相同,C可发生银镜反应.它们之间的转化关系如图(部分反应条件和产物略去).请回答:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质量数是177 | B. | 中子数是117 | C. | 核外电子数117 | D. | 质子数是177 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl溶于水能电离出H+、Cl-,所以HCl是离子化合物 | |
| B. | 碘晶体受热转变成碘蒸气,吸收的热量用于克服碘原子间的作用力 | |
| C. | He、CO2和CH4都是由分于构成,它们中都存在共价键 | |
| D. | NaHCO3受热分解生成Na2CO3、CO2和H2O,旣破坏了离子键,也破坏了共价键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com