
【题目】下列说法中错误是的( )
A.含有共价键的化合物一定是共价化合物
B.在共价化合物中一定含有共价键
C.含有离子键的化合物一定是离子化合物
D.双原子单质分子中含有的共价键一定非极性共价键
 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源: 题型:
【题目】原子结构与元素周期表存在着内在联系,根据已学知识请你回答下列问题。
(1)指出31号元素镓(Ga)在元素周期表中的位置:第_______周期______族。
(2)写出原子序数最小的Ⅷ族元素原子的核外电子排布式:_____________________________。
(3)写出3p轨道上只有2个未成对电子的元素的符号:________、________,二者电负性________>________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、科技、医药、工业生产均密切相关,下列有关化学叙述正确的是
A. “大漠孤烟直”描述的是物质升华的过程
B. 《本草经集注》中关于鉴别硝石(KNO3)和朴硝(Na2SO4)的记载:“以火烧之,紫青烟起,乃真硝石也”,该方法应用了焰色反应
C. 误食重金属盐引起的人体中毒,可喝大量的食盐水解毒
D. ![]() 表示一种高分子树脂,因难溶于水,不具备吸水性
表示一种高分子树脂,因难溶于水,不具备吸水性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,往水中不断加入NaHC2O4固体,部分微粒浓度随加入的c(HC2O4-)的变化趋势如下图所示。下列说法正确的是( )

A. 当c(HC2O4-)=0.1mol/L时,c(H+)>c(C2O42-)-c(H2C2O4)
B. 当c(HC2O4-)>amol/L时,c(H+)< c(H2C2O4),HC2O4-的水解程度大于电离程度
C. HC2O4-![]() C2O42-+H+,Ka(HC2O4-)=a
C2O42-+H+,Ka(HC2O4-)=a
D. 将0.08mo1/L H2C2O4溶液与等浓度NaOH溶液等体积混合后(忽略体积变化),c(Na+)>c(HC2O4-)>c(C2O42-)>c(H2C2O4)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质在水溶液中关于电离方程式错误的是
A. MgCl2 = Mg2+ + 2Cl
B. Ba(OH)2 = Ba2+ + 2OH
C. CH3COOH = H+ + CH3COO-
D. KHSO4 = K+ + H+ + SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油裂解气用途广泛,可用于合成各种橡胶和医药中间体。利用石油裂解气合成CR橡胶和医药中间体K的线路如下:
已知: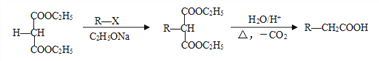
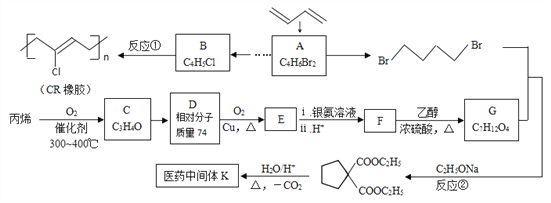
(1)A的反式异构体的结构简式为____________________ 。
(2)用系统命名法给B命名,其名称是__________________。
(3)依次写出①、②的反应类型、____________ 、____________。
(4)C、D、E均为链状结构,且均能与新制氢氧化铜悬浊液共热生成砖红色沉淀,则C中含有的官能团名称是________________________。 写出反应D→E的化学方程式_______________________________________________________。
(5)K的结构简式为_____________________________。
(6)写出F与乙二醇发生聚合反应的化学方程式___________________________________。
(7)写出同时满足下列条件的医药中间体K的所有同分异构体的结构简式_____________。
a.与E互为同系物 b.核磁共振氢谱有3种峰
(8)已知双键上的氢原子很难发生取代反应。以A为起始原料,选用必要的无机试剂合成B,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以熔融Na2CO3为电解质,H2和CO混合气为燃料的电池原理如图所示。下列说法正确的是( )
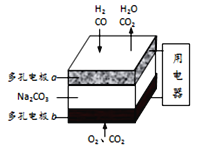
A. b是电池的负极
B. 该电池使用过程中需补充Na2CO3
C. a、b两级消耗气体的物质的量之比为2:1
D. 电极a上每消耗22.4L原料气体,电池中转移电子数约为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既属于氧化还原反应,又是吸热反应的是( )
A.锌粒与稀硫酸的反应
B.水分解生成氢气和氧气
C.甲烷在空气中燃烧的反应
D.Ba(OH)28H2O晶体与NH4Cl晶体的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、E、F、G七种元素为周期表中原子序数依次增大的前四周期元素。6X的一种核素能用于测定文物的年代;Y元素最高价氧化物对应水化物能与其常见氢化物反应生成盐M;Z原子核外成对电子数是未成对电子数的3倍;W的原子半径在同周期主族元素中最大;E的基态原子的所有电子位于四个能级且每个能级均全充满;F的电负性在同周期中最大;G的基态原子N层只有一个电子,内层电子全部排满。请回等下列问题: (用X、Y、Z、W、E、F、G所对应的元素符号表示)
(1)写山F的基态原子的核外电子排布式:______________。
(2)Y、Z、W的电负性由大到小的顺序为_____________。
(3)以下可以表示X的基态原子的原子轨道表示式的是____________。
A. ![]() B.
B. ![]() C.
C. ![]()
(4)下图可以表示F的氢化物中电子云重叠方式的是_______。
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
(5)基态E原子核外存在_____种运动状态不同的电子。
(6)G元素位于周期表中的_____区,基态原子价电子排布式为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com