
(13分)下图中A~K分别代表有关反应的一种反应物或生成物,其中A、C、F、K是固体。已知A是一种不含金属元素的盐,受热分解得到三种产物物质的量之比为2︰1︰1;A加热后生成的混合气体若通过碱石灰,只剩余气体B(B为无色有刺激性气味的气体),若通过浓硫酸则只剩余气体D(D为无色无味气体);C为淡黄色固体。各物质间的转化关系如下图所示:
请回答:
(1)D中化学键的类型为________,C的电子式 ,B的空间构型为_________。
(2)写出A的溶液与足量NaOH溶液反应的离子方程式 。
(3)写出J与K反应的化学方程式 。
(4)在标准状况下4.48L的H与I恰好被100mlNaOH溶液完全吸收,所需NaOH溶液的物质的量浓度
为 mol·L-1。
(5)工业尾气中含有各种氮的氧化物(主要是NO和NO2,表示为NOx),NOx是严重的大气污染物,处理这些废气方法之一是通入适量的B,反应后会生成一种无色无味的气体。写出NOx与B反应的化学方程式______________________________。
(13分)
(1)共价键(1分)  (2分) 三角锥形(2分)
(2分) 三角锥形(2分)
(2)NH4++OH-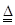 2NH3 ↑+ H2O (或NH4++ OH-="=" NH3·H2O) (2分)
2NH3 ↑+ H2O (或NH4++ OH-="=" NH3·H2O) (2分)
(3)C+4HNO3(浓)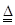 4NO2 ↑+ CO2 ↑+2H2O (2分)
4NO2 ↑+ CO2 ↑+2H2O (2分)
(4)2mol·L-1
(5)2NH3+NO2+NO====2N2+3H2O或4xNH3+6NOx="===" (2x+3)N2+6xH2O(2分)
解析试题分析:A是一种不含金属元素的盐,受热分解得到三种产物物质的量之比为2︰1︰1;可知该盐为铵盐,酸根为二元弱酸的酸根,应为碳酸铵;A加热后生成的混合气体若通过碱石灰,只剩余气体B(B为无色有刺激性气味的气体),气体B为NH3;若通过浓硫酸则只剩余气体D(D为无色无味气体,D为CO2;C为淡黄色固,且与二氧化碳反应,C为Na2O2生成E、F,F是固,则E为O2,F为Na2CO3;B NH3与E O2反应生成G、H,则G为水,H为NO;I为NO2,J为HNO3,K为固体,燃烧生成二氧化碳D,则K为C ;(1)CO2中化学键的类型为共价键,Na2O2的电子式 ,NH3的空间构型为三角锥形;(2)碳酸铵溶液与足量NaOH溶液反应的离子方程式NH4++OH-
,NH3的空间构型为三角锥形;(2)碳酸铵溶液与足量NaOH溶液反应的离子方程式NH4++OH-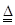 2NH3 ↑+ H2O (或NH4++ OH-="=" NH3·H2O); (3)HNO3与C反应的化学方程C+4HNO3(浓)
2NH3 ↑+ H2O (或NH4++ OH-="=" NH3·H2O); (3)HNO3与C反应的化学方程C+4HNO3(浓)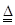 4NO2 ↑+ CO2 ↑+2H2O ;(4)在标准状况下4.48L的NO与NO2恰好被100mlNaOH溶液完全吸收,由元素守恒可知N元素为0.2mol,则所需NaOH的物质的量为0.2mol,溶液的物质的量浓度为2mol?L-1;(5)NOx与NH3反应的化学方程式2NH3+NO2+NO====2N2+3H2O或4xNH3+6NOx="===" (2x+3)N2+6xH2O。
4NO2 ↑+ CO2 ↑+2H2O ;(4)在标准状况下4.48L的NO与NO2恰好被100mlNaOH溶液完全吸收,由元素守恒可知N元素为0.2mol,则所需NaOH的物质的量为0.2mol,溶液的物质的量浓度为2mol?L-1;(5)NOx与NH3反应的化学方程式2NH3+NO2+NO====2N2+3H2O或4xNH3+6NOx="===" (2x+3)N2+6xH2O。
考点:元素化合物知识应用、无机推断


科目:高中化学 来源: 题型:单选题
下列物质中不能用化合反应的方法制得的是
①SiO2 ②H2SiO3 ③Fe(OH)3 ④Al(OH)3 ⑤FeCl2 ⑥ CaSiO3
| A.①③ | B.②④ | C.②③④⑤ | D.②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
(9分)甲、丙、丁是由短周期元素组成的物质,它们之间存在如下转化关系。
甲 + H2O → 丙 + 丁
(1)转化关系中所涉及的反应为非氧化还原反应。
①若甲是一种钠盐,丁为两性氢氧化物,则甲的化学式为 ,丁的酸式电离方程式为 。
②若甲是由N和Cl元素组成的化合物,其分子结构模型如图所示,丙具有漂白性。则甲中Cl元素的化合价是 ,丁与H2O有相同的电子总数,则丁的电子式为 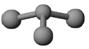
(2)转化关系中所涉及的反应为氧化还原反应。
①若甲和丙是同主族元素组成的单质,且组成甲的元素位于第三周期,此反应的离子方程式是 。
②若丙和丁都可在一定条件下还原CuO,此反应的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
(10分)已知A~H是中学化学中的常见物质,A、C、G是金属,E、F是氧化物,B溶于水得蓝色溶液,它们有如下图所示的关系(反应中生成的水已略去)。
试回答下列问题。
(1)推断填写物质化学式:A是 ,D是 ,H是 。
(2)F的类别是 (选填“酸性氧化物”、“碱性氧化物”或“两性氧化物”)。
(3)反应④的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
(6分)下图所示各物质是由短周期部分元素组成的单质或其化合物,图中部分反应条件及物质未列出。已知:A、C、D、F均为单质,C、E、F、G常温下是气体,J为白色沉淀,既能溶于B,又能溶于E;物质B、G可以使湿润的红色石蕊试纸变蓝,且B的焰色反应呈黄色。反应④是化肥工业的重要反应。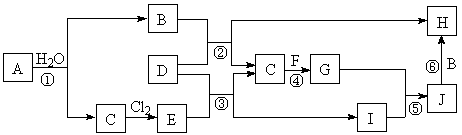
请回答下列问题:
(1)A的元素在元素周期表中的位置是 ,物质B的电子式为 。
(2)上述反应①~⑥中,属于化合反应的是 ,反应⑤的离子方程式为 。
(3)在I的水溶液滴加B溶液至过量的过程中,所观察到的现象为 。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
化学反应伴随能量变化,下列说法中错误的是
| A.TNT(炸药)爆炸时部分化学能转化为热能 |
| B.电解饱和食盐水时部分化学能转化为电能 |
| C.镁条燃烧时部分化学能转化为光能 |
| D.植物光合作用时部分光能转化为化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
实验题:(共15分)
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯。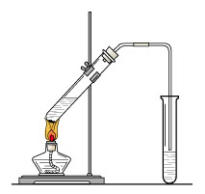
回答下列问题:
(1)写出制取乙酸乙酯的化学反应方程式
(2)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合液的方法是 。
(3)浓硫酸的作用是:① ; ② 。
(4)饱和碳酸钠溶液的主要作用是
(5)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止 。
(6)若要把制得的乙酸乙酯分离出来,应采用的实验操作是 。
(7)做此实验时,有时还向盛乙酸和乙醇的试管里加入几块碎瓷片,其目的是 。
(8)生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,也即达到化学平衡状态。下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号) 。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④正反应的速率与逆反应的速率相等
⑤混合物中各物质的浓度不再变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com