
 £»
£»·ÖĪö £Ø1£©øł¾Żn=$\frac{m}{M}$¼ĘĖćÓŠ»śĪļA”¢¶žŃõ»ÆĢ¼”¢Ė®µÄĪļÖŹµÄĮ棬øł¾ŻŌ×ÓŹŲŗć¼ĘĖćĢž·Ö×ÓÖŠC”¢HŌ×ÓŹżÄ棬øł¾ŻĻą¶ŌŌ×ÓÖŹĮæ¼ĘĖć·Ö×ÓÖŠŃõŌ×ÓŹżÄ棬¾Ż“ĖŹéŠ“øĆĢžµÄ·Ö×ÓŹ½£»
£Ø2£©ŗģĶā¹āĘ×·ÖĪö±ķĆ÷A·Ö×ÓÖŠŗ¬ÓŠO-H¼üŗĶĪ»ÓŚ·Ö×Ó¶ĖµÄC”ŌC¼ü£¬ŗĖ“Ź²ÕńĒāĘ×ÓŠČżøö·å£¬·åĆ껿ĪŖ6£ŗ1£ŗ1£¬·Ö×ÓÖŠÓŠ3ÖÖ²»Ķ¬µÄHŌ×Ó£¬Ō×ÓŹżÄæÖ®±ČĪŖ6£ŗ1£ŗ1£¬½įŗĻÓŠ»śĪļµÄ·Ö×ÓŹ½ÅŠ¶ĻÓŠ»śĪļAµÄ½į¹¹£»
£Ø3£©øł¾ŻÓŠ»śĪļAŗ¬ÓŠŹĒ¹ŁÄÜĶŽųŠŠ·ÖĪö½ā“š£»
£Ø4£©ÓŠ»śĪļBŹĒAµÄĶ¬·ÖŅģ¹¹Ģ壬1molBæÉÓė1molBr2¼Ó³É£¬¹Ź·Ö×ÓÖŠŗ¬ÓŠ1øöC=CĖ«¼ü£¬øĆÓŠ»śĪļĖłÓŠĢ¼Ō×ÓŌŚĶ¬Ņ»øöĘ½Ćę£¬ĘäÓąµÄĢ¼Ō×ÓĮ¬½ÓC=CĖ«¼ü£¬Ć»ÓŠĖ³·“Ņģ¹¹ĻÖĻ󣬲»±„ŗĶĖ«¼üÖĮÉŁĘäÖŠŅ»øöCŌ×ÓĮ¬½ÓĮ½øöĻąĶ¬µÄ»łĶż׻ł£¬½įŗĻAµÄ½į¹¹¼ņŹ½ŹéŠ“£®
½ā“š ½ā£ŗ£Ø1£©ÓŠ»śĪļAÖ»ŗ¬ÓŠC”¢H”¢OČżÖÖŌŖĖŲ£¬ÖŹĘ×Ķ¼±ķĆ÷ĘäĻą¶Ō·Ö×ÓÖŹĮæĪŖ84£¬16.8gÓŠ»śĪļAµÄĪļÖŹµÄĮæ=$\frac{16.8g}{84g/mol}$=0.2mol£¬¾Č¼ÉÕÉś³É44.0g CO2£¬ĪļÖŹµÄĮæĪŖ1mol£¬Éś³É14.4g H2O£¬ĪļÖŹµÄĮæĪŖ $\frac{14.4g}{44g/mol}$=0.8mol£¬¹ŹÓŠ»śĪļA·Ö×ÓÖŠN£ØC£©=$\frac{1mol”Į1}{0.2mol}$=5£¬N£ØH£©=$\frac{0.8mol”Į2}{0.2mol}$=8£¬¹ŹN£ØO£©=$\frac{84-12”Į5-8}{16}$=1£¬¹ŹAµÄ·Ö×ÓŹ½ĪŖC5H8O£¬
¹Ź“š°øĪŖ£ŗC5H8O£»
£Ø2£©²»±„ŗĶ¶ČĪŖ£ŗ$\frac{2”Į5+2-8}{2}$=2£¬ŗģĶā¹āĘ×·ÖĪö±ķĆ÷A·Ö×ÓÖŠŗ¬ÓŠO-H¼üŗĶĪ»ÓŚ·Ö×Ó¶ĖµÄC”ŌC¼ü£¬ŗĖ“Ź²ÕńĒāĘ×ÓŠČżøö·å£¬·åĆ껿ĪŖ6£ŗ1£ŗ1£¬¹Ź·Ö×ÓÖŠŗ¬ÓŠ2øöCH3”¢1øö-OHĮ¬½ÓŌŚĶ¬Ņ»CŌ×ÓÉĻ£¬ĖłŅŌAµÄ½į¹¹¼ņŹ½ĪŖ£ŗ £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£»
£Ø3£©ŗģĶā¹āĘ×·ÖĪö±ķĆ÷A·Ö×ÓÖŠŗ¬ÓŠO-H¼üŗĶĪ»ÓŚ·Ö×Ó¶ĖµÄC”ŌC¼ü£¬²»±„ŗĶ¶ČĪŖ£ŗ$\frac{2”Į5+2-8}{2}$=2£¬²»ŗ¬ĘäĖü¹ŁÄÜĶÅ£¬ŗ¬ÓŠōĒ»ł£¬ÄÜÓėÄĘ·“Ó¦£¬ŗ¬ÓŠC”ŌCĖ«¼ü£¬ÄÜÓėĖįŠŌøßĆĢĖį¼Ų·¢ÉśŃõ»Æ·“Ó¦£¬ÄÜÓėäå·¢Éś¼Ó³É·“Ó¦£¬ÄÜÓėĒāĘų·¢Éś¼Ó³É·“Ó¦£¬ÄÜÓėNaOHČÜŅŗ·“Ó¦£¬
¹Ź“š°øĪŖ£ŗabcd£»
£Ø4£©ÓŠ»śĪļBŹĒAµÄĶ¬·ÖŅģ¹¹Ģ壬1molBæÉÓė1molBr2¼Ó³É£¬¹Ź·Ö×ÓÖŠŗ¬ÓŠ1øöC=CĖ«¼ü£¬øĆÓŠ»śĪļĖłÓŠĢ¼Ō×ÓŌŚĶ¬Ņ»øöĘ½Ćę£¬ĘäÓąµÄĢ¼Ō×ÓĮ¬½ÓC=CĖ«¼ü£¬Ć»ÓŠĖ³·“Ņģ¹¹ĻÖĻ󣬲»±„ŗĶĖ«¼üÖĮÉŁĘäÖŠŅ»øöCŌ×ÓĮ¬½ÓĮ½øöĻąĶ¬µÄ»łĶż׻ł£¬½įŗĻAµÄ½į¹¹¼ņŹ½æÉÖŖ£¬BÖŠ»¹ŗ¬ÓŠ-CHO£¬¹ŹBµÄ½į¹¹¼ņŹ½ĪŖ£ŗ£©£ØCH3£©2C=CHCHO£¬
¹Ź“š°øĪŖ£ŗ£ØCH3£©2C=CHCHO£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļµÄĶʶĻ£¬Éę¼°·Ö×ÓŹ½”¢½į¹¹Ź½µÄČ·¶Ø”¢¹ŁÄÜĶÅŠŌÖŹ”¢Ķ¬·ÖŅģ¹¹ĢåŹéŠ“µČÖŖŹ¶£¬ĢāÄæÄѶČÖŠµČ£¬ŹĒ¶Ōѧɜ×ŪŗĻÄÜĮ¦µÄæ¼²é£¬Č·¶Ø·Ö×ÓŹ½ŹĒ½āĢāµÄ¹Ų¼ü£¬×¢ŅāÕĘĪÕ³£¼ūÓŠ»śĪļ½į¹¹ÓėŠŌÖŹ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ō×Ó°ė¾¶£ŗW£¾X£¾Y | |
| B£® | XµÄµ„ÖŹ²»ÄÜÓėZµÄŃõ»ÆĪļ·“Ó¦ | |
| C£® | WµÄµ„ÖŹŌŚYµÄµ„ÖŹÖŠČ¼ÉÕ²śÉśµĄ¶É«»šŃę | |
| D£® | X”¢YæÉŠĪ³É¼ČÓŠĄė×Ó¼üÓÖÓŠ¹²¼Ū¼üµÄĄė×Ó»ÆŗĻĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
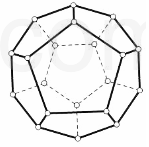 2000 Äź£¬µĀ¹śFreiburg“óѧµÄH£®PrinzbachŠū³Ę£¬ĖūĆĒĶعżÕŖ³ż·Ø£¬ŅŃ¾ŌŚĘųĻąÖŹĘ×ŅĒµÄĘųĢåÖŠ·¢ĻÖĮĖ×īŠ”µÄĒņĢ¼·Ö×Ó£Øø»ĄÕĻ©£©--C20£ØČēĶ¼ĖłŹ¾£©£®Č»ŗóŌŚµē×Ó³å»÷ÖŹĘ×ŅĒÖŠ¹Ū²ģµ½ĮĖĪ¢ĮæC20+ŗĶC202+µÄ“ęŌŚ£® Ėū½«C20H20 ČܽāŌŚŅŗäåĄļ£¬ŌŚÉÕĘæĄļ¼ÓŃ¹³¤Ź±¼ä»ŲĮ÷£¬×īÖÕµĆµ½Ę½¾ł×é³ÉĪŖ C20HBr13µÄ²śĪļ£®
2000 Äź£¬µĀ¹śFreiburg“óѧµÄH£®PrinzbachŠū³Ę£¬ĖūĆĒĶعżÕŖ³ż·Ø£¬ŅŃ¾ŌŚĘųĻąÖŹĘ×ŅĒµÄĘųĢåÖŠ·¢ĻÖĮĖ×īŠ”µÄĒņĢ¼·Ö×Ó£Øø»ĄÕĻ©£©--C20£ØČēĶ¼ĖłŹ¾£©£®Č»ŗóŌŚµē×Ó³å»÷ÖŹĘ×ŅĒÖŠ¹Ū²ģµ½ĮĖĪ¢ĮæC20+ŗĶC202+µÄ“ęŌŚ£® Ėū½«C20H20 ČܽāŌŚŅŗäåĄļ£¬ŌŚÉÕĘæĄļ¼ÓŃ¹³¤Ź±¼ä»ŲĮ÷£¬×īÖÕµĆµ½Ę½¾ł×é³ÉĪŖ C20HBr13µÄ²śĪļ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | F | B£® | Mg | C£® | Al | D£® | Si |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
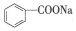 £¬ĖõŠ“ĪŖNaA£©æÉÓĆ×÷ŅūĮĻµÄ·ĄøƼĮ£®ŃŠ¾æ±ķĆ÷±½¼×Ėį£ØHA£©µÄŅÖ¾śÄÜĮ¦ĻŌÖųøßÓŚA-£®ŅŃÖŖ25”ꏱ£¬HAµÄKa=6.25”Į10-5£¬H2CO3µÄKa1=4.17”Į10-7£¬Ka2=4.90”Į10-11£®ŌŚÉś²śĢ¼ĖįŅūĮĻµÄ¹ż³ĢÖŠ£¬³żĮĖĢķ¼ÓNaAĶā£¬»¹Šč¼ÓŃ¹³äČėCO2ĘųĢ壮ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£ØĪĀ¶ČĪŖ25”ę£¬²»æ¼ĀĒŅūĮĻÖŠĘäĖū³É·Ö£©£Ø””””£©
£¬ĖõŠ“ĪŖNaA£©æÉÓĆ×÷ŅūĮĻµÄ·ĄøƼĮ£®ŃŠ¾æ±ķĆ÷±½¼×Ėį£ØHA£©µÄŅÖ¾śÄÜĮ¦ĻŌÖųøßÓŚA-£®ŅŃÖŖ25”ꏱ£¬HAµÄKa=6.25”Į10-5£¬H2CO3µÄKa1=4.17”Į10-7£¬Ka2=4.90”Į10-11£®ŌŚÉś²śĢ¼ĖįŅūĮĻµÄ¹ż³ĢÖŠ£¬³żĮĖĢķ¼ÓNaAĶā£¬»¹Šč¼ÓŃ¹³äČėCO2ĘųĢ壮ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£ØĪĀ¶ČĪŖ25”ę£¬²»æ¼ĀĒŅūĮĻÖŠĘäĖū³É·Ö£©£Ø””””£©| A£® | Ļą±ČÓŚĪ“³äCO2µÄŅūĮĻ£¬Ģ¼ĖįŅūĮĻµÄŅÖ¾śÄÜĮ¦½ĻµĶ | |
| B£® | ĢįøßCO2³äĘųŃ¹Į¦£¬ŅūĮĻÖŠc£ØA-£©²»±ä | |
| C£® | µ±pHĪŖ5.0Ź±£¬ŅūĮĻÖŠ$\frac{c£ØHA£©}{c£Ø{A}^{-}£©}$=0.16 | |
| D£® | Ģ¼ĖįŅūĮĻÖŠø÷ÖÖĮ£×ÓµÄÅØ¶Č¹ŲĻµĪŖ£ŗc£ØH+£©=c£ØHCO${\;}_{3}^{-}$£©+2c£ØCO${\;}_{3}^{2-}$£©+c£ØOH-£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ·śŹĒ×ŌČ»½ēÖŠ¹ć·ŗ·Ö²¼µÄŌŖĖŲÖ®Ņ»£®ÓÉÓŚ·śµÄĢŲŹā»ÆѧŠŌÖŹ£¬ĖüŗĶĘäĖūĀ±ĖŲŌŚµ„ÖŹ¼°»ÆŗĻĪļµÄÖʱøÓėŠŌÖŹÉĻ“ęŌŚ½ĻĆ÷ĻŌµÄ²īŅģ£®
·śŹĒ×ŌČ»½ēÖŠ¹ć·ŗ·Ö²¼µÄŌŖĖŲÖ®Ņ»£®ÓÉÓŚ·śµÄĢŲŹā»ÆѧŠŌÖŹ£¬ĖüŗĶĘäĖūĀ±ĖŲŌŚµ„ÖŹ¼°»ÆŗĻĪļµÄÖʱøÓėŠŌÖŹÉĻ“ęŌŚ½ĻĆ÷ĻŌµÄ²īŅģ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĒāŃõ»ÆĀĮæÉ×÷ĪøĖįµÄÖŠŗĶ¼Į | B£® | ¹¤ŅµÉĻ²ÉÓƵē½āČŪČŚĀČ»ÆĀĮÖĘĀĮ | ||
| C£® | ĀĮ¹ŽæÉ¾ĆŹ¢Ź³“× | D£® | Ć÷·ÆÓĆ×÷¾»Ė®¼Į²»Éę¼°»Æѧ±ä»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £¼
£¼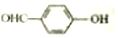
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com