
| A. | H2O(g)=H2(g)+$\frac{1}{2}$ O2(g)△H=+242 kJ/mol | B. | 2 H2(g)+O2(g)=2 H2O(g)△H=-484 kJ/mol | ||
| C. | H2(g)+$\frac{1}{2}$ O2(g)=H2O(g)△H=+242 kJ/mol | D. | 2 H2(g)+O2(g)=2 H2O(g)△H=+484 kJ/mol |
分析 书写或判断热化学方程式应注意以下三点:①热化学方程式的右侧注明热量的变化,△H<0放热,△H>0吸热.②注明各物质的聚集状态(气-g,液-l,固-s),③各物质前面的系数表示物质的量,由此分析解答.
解答 解:A、1mol氢气完全燃烧生成水蒸气时放出的热量为:484 kJ÷2=242 kJ,由于H2O的分解与化合,反应方向相反,故吸热与放热的数值相等,故A正确;
B、表示2mol氢气燃烧生成水蒸气放出484kJ热量,故B正确;
C、是放热反应,△H<0,故C错误;
D、氢气在氧气中燃烧是放热反应,所以△H<0,故D错误;
故选AB.
点评 本题是考查热化学方程式的书写的正误判断,学生只要掌握书写热化学方程的注意点,就可以迅速解题,比较容易.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
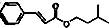 )是一种香料,一种合成路线如下:
)是一种香料,一种合成路线如下: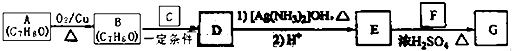 已知以下信息:
已知以下信息: ;
; +CH3CHO$\stackrel{一定条件}{→}$
+CH3CHO$\stackrel{一定条件}{→}$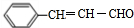 +H2O.
+H2O. +(CH3)2CHCH2CH2OH$→_{△}^{浓硫酸}$
+(CH3)2CHCH2CH2OH$→_{△}^{浓硫酸}$ +H2O,反应类型为酯化反应.
+H2O,反应类型为酯化反应.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 | |
| B. | 由H+(aq)+OH-(aq)=H2O(I);△H=-57.3kJ•mol-1molCH3COOH的稀溶液与含l mol NaOH的稀溶液混合,放出的热量小于57.3 kJ | |
| C. | 由C(石墨)=(金刚石);△H=+1.90kJ•mol-1可知,金刚石比石墨稳定 | |
| D. | 500℃、30MPa下,将0.5 mol(g)和1.5 mol (g)置于密闭容器中充分反应生成(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g);△H=-38.6kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16 | B. | 14 | C. | 12 | D. | 28 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
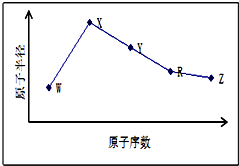 W、X、Y、Z、R是五种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10.X和Ne原子的核外电子数相差1.Y的最高价氧化物对应水化物是医用胃酸中和剂中的一种.R和W具有相同的最外层电子数.Z在同周期主族元素中原子半径最小.
W、X、Y、Z、R是五种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10.X和Ne原子的核外电子数相差1.Y的最高价氧化物对应水化物是医用胃酸中和剂中的一种.R和W具有相同的最外层电子数.Z在同周期主族元素中原子半径最小.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
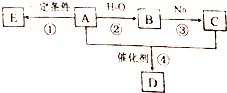 气体A是石油裂解的主要产物之一,其相对分子质量为28,C是一中气体,E是一种高分子化合物.A、B、C、D、E在一定条件下存在如图转化关系(部分反应条件、产物被省略)
气体A是石油裂解的主要产物之一,其相对分子质量为28,C是一中气体,E是一种高分子化合物.A、B、C、D、E在一定条件下存在如图转化关系(部分反应条件、产物被省略)查看答案和解析>>
科目:高中化学 来源: 题型:选择题


| A. | 合成过程涉及加成、消去、酯化、聚合等类型的有机反应 | |
| B. | 步骤(1)中②反应发生的条件是在NaOH/醇溶液中加热,反应类型是消去反应 | |
| C. | 步骤(1)(2)连续操作时,③、⑤消耗H2物质的量相等 | |
| D. | ⑥反应方程式中产物H2O系数x=2,及时除去⑥中反应釜内的水可提高DEHP产率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com