
| A. | 反应①是加成反应,反应⑧是消去反应,其它所标明的反应都是取代反应 | |
| B. | 上述物质中能与NaOH溶液反应的只有乙酸 | |
| C. | 1,2一二溴乙烷、乙烯、乙醇烃基上的氢被氯取代,其一氯取代产物都是一种 | |
| D. | 等物质的量的乙烯和乙醇与足量氧气反应时耗氧量相同 |
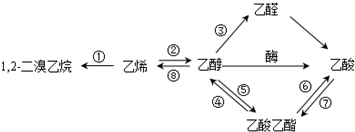
分析 由转化关系可知,乙烯与溴发生加成反应1,2-二溴乙烷,乙烯与水发生加成反应生成乙醇,乙醇催化氧化为乙醛,乙酸乙酯水解生成乙醇和乙酸,乙醇与乙酸酯化反应生成乙酸乙酯,乙醇发生消去反应生成乙烯,以此来解答.
解答 解:由转化关系可知,乙烯与溴发生加成反应1,2-二溴乙烷,乙烯与水发生加成反应生成乙醇,乙醇催化氧化为乙醛,乙酸乙酯水解生成乙醇和乙酸,乙醇与乙酸酯化反应生成乙酸乙酯,乙醇发生消去反应生成乙烯,
A.①②为加成反应,⑧为消去反应,③为氧化反应,其它所标明的反应都是取代反应,故A错误;
B.1,2-二溴乙烷、乙酸、乙酸乙酯均与NaOH反应,故B错误;
C.乙醇烃基上的氢有2种,则一氯取代产物有2种,故C错误;
D.等物质的量的乙烯和乙醇与足量氧气反应时,对应有机物CxHyOz,由x+$\frac{y}{4}$-$\frac{z}{2}$可知,耗氧量相同,故D正确;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、常见有机物的性质为解答的关键,注意分析转化中发生的反应及有机物结构对称性,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
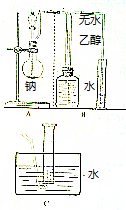 乙醇的分子式为C2H6O,有人设计了如图所示的实验来确定乙醇分子的结构.
乙醇的分子式为C2H6O,有人设计了如图所示的实验来确定乙醇分子的结构.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 一定温度和电压下,电解精制食盐水可制取NaClO3.电解装置如图.已知:3Cl2+6OH-=ClO3-+5Cl-+3H2O.下列说法正确的是( )
一定温度和电压下,电解精制食盐水可制取NaClO3.电解装置如图.已知:3Cl2+6OH-=ClO3-+5Cl-+3H2O.下列说法正确的是( )| A. | 铁为阳极,电极反应式为2H2O+2e-=H2↑+2OH- | |
| B. | 若阴极产生3.36L(标况)气体,则溶液中的反应转移电子0.30mol | |
| C. | 电解槽内总反应方程式为:NaCl+3H2O $\frac{\underline{\;通电\;}}{\;}$NaClO3+3H2↑ | |
| D. | 用阳离子交换膜代替阴离子交换膜,也一样可以制得NaClO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
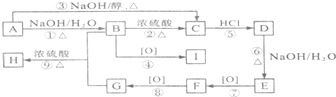
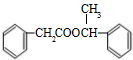 .
. +NaOH$→_{△}^{水}$
+NaOH$→_{△}^{水}$ +NaCl.
+NaCl.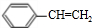 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$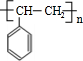 .
.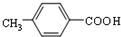 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

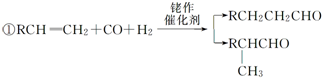
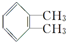 ,名称为邻二甲苯.
,名称为邻二甲苯.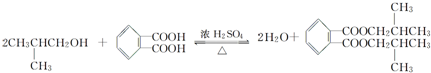 .
.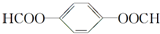 ;X分子中有2种不同化学环境的氢原子,其峰面积之比为1:2;1mol X与NaOH溶液共热反应,最多消耗4 mol NaOH.
;X分子中有2种不同化学环境的氢原子,其峰面积之比为1:2;1mol X与NaOH溶液共热反应,最多消耗4 mol NaOH.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2:1 | B. | 3:1 | C. | 1:1 | D. | 4:5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
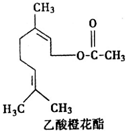
| A. | 分子式为C12H20O2 | |
| B. | 能使酸性KMnO4溶液褪色 | |
| C. | 能发生加成反应,但不能发生取代反应 | |
| D. | 1mol该有机物水解时只能消耗lmolNaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,11.2LN2和NO的混合气体所含的原子数为NA | |
| B. | 1mol C8H18分子中,共价键总数为25NA | |
| C. | 标准状况下,22.4L盐酸含有nA个HCl分子 | |
| D. | 含0.1molH2O2的水溶液跟MnO2充分作用,反应过程中转移的电子总数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com