
 2NO2(g) ΔH= +57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法错误的是
2NO2(g) ΔH= +57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法错误的是 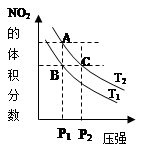
 2NO2(g) ΔH= +57kJ·mol-1,从这可以看出,该反应为吸热反应,所以温度升高,平衡向正反应方向移动,故颜色加深;减小压强,平衡向正反应方向移动,颜色加深,从图中可以看出,T1<T2,P1< P2,图中C点可以通过A点加压而得到,B点很明显的颜色小于C点,故A、B、C三点中气体 颜色最深的为C点,故A正确,维持压强不变,由B点到A点保持压强不变,升高温度的过程,所以反应向正方向进行,故B正确,C点可以通过A点加压而得到,所以A、C两点的反应速率为A<C,故C错误,为本题的答案;B、C两点化学平衡常数:B<C,因为温度高,平衡常数大。
2NO2(g) ΔH= +57kJ·mol-1,从这可以看出,该反应为吸热反应,所以温度升高,平衡向正反应方向移动,故颜色加深;减小压强,平衡向正反应方向移动,颜色加深,从图中可以看出,T1<T2,P1< P2,图中C点可以通过A点加压而得到,B点很明显的颜色小于C点,故A、B、C三点中气体 颜色最深的为C点,故A正确,维持压强不变,由B点到A点保持压强不变,升高温度的过程,所以反应向正方向进行,故B正确,C点可以通过A点加压而得到,所以A、C两点的反应速率为A<C,故C错误,为本题的答案;B、C两点化学平衡常数:B<C,因为温度高,平衡常数大。

 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源:不详 题型:单选题
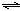 W(g) + Z(g),下列物理量不能用于表明反应是否已达到平衡状态的是
W(g) + Z(g),下列物理量不能用于表明反应是否已达到平衡状态的是| A.Y的物质的量浓度 |
| B.混合气体的密度 |
| C.混合气体的压强 |
| D.混合气体的平均相对分子量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 H2S(g) K1,
H2S(g) K1, SO2(g) K2。则相同温度下反应H2(g)+SO2(g)
SO2(g) K2。则相同温度下反应H2(g)+SO2(g)  O2(g)+H2S(g)的
O2(g)+H2S(g)的| A.K1+K2 | B.K1-K2 | C.K1·K2 | D.K1/K2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
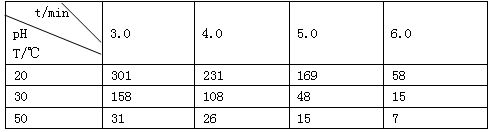
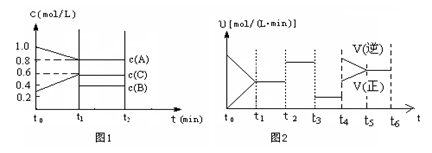
| 时间段 | t1~t2 | t2~t3 | t3~t4 | t5~t6 |
| 平衡常数 | K1 | K2 | K3 | K4 |
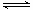 CH3OH(g)反应合成甲醇。
CH3OH(g)反应合成甲醇。| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
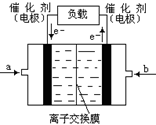
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 B+C,在某一温度时,达到平衡。
B+C,在某一温度时,达到平衡。 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3(g),若N2、H2、NH3的起始浓度分别为C1、C2、C3(均不为零),到达平衡时,N2、H2、NH3的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.08 mol·L-1,则下列判断正确的是( )
2NH3(g),若N2、H2、NH3的起始浓度分别为C1、C2、C3(均不为零),到达平衡时,N2、H2、NH3的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.08 mol·L-1,则下列判断正确的是( )| A.C1:C2=1:3 |
| B.平衡时,H2和NH3的生成速率之比为2:3 |
| C.N2、H2的转化率之比为1:3 |
| D.C1的取值范围为0.04 mol·L-1<C1<0.14 mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.当一个可逆反应达到平衡状态时,就是这个反应在该条件下所能达到的限度 |
| B.当一个可逆反应达到平衡状态时,这个反应的正反应速率和逆反应速率相等 |
C.对反应N2+3H2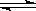 2NH3而言,无论怎样控制反应条件1mol N2与3mol H2反应都不会生成2mol NH3 2NH3而言,无论怎样控制反应条件1mol N2与3mol H2反应都不会生成2mol NH3 |
| D.化学反应的限度不可以通过改变条件来改变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0molS02 | B.2mol S03 | C.1mol 02 | D.1molSO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com