
【题目】过氧化氢被称为绿色氧化剂,它的分子结构如下图所示。已知该分子H-O-O键角都是97°。下列有关H2O2的说法正确的是
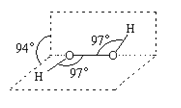
A.过氧化氢分子中存在离子键、共价键
B.在1.00mol H2O2中,核外电子总数为10×6.02×1023个
C.过氧化氢既有氧化性又有还原性
D.3.4g过氧化氢中含有6.02×1022个原子
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:
【题目】以磷灰石(一类含钙的磷酸盐矿物总称)原料生产磷铵的工艺流程图如下:
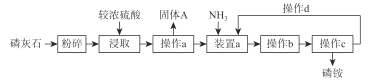
已知:纯的磷酸铵盐为白色晶体,其中以磷酸一铵最稳定,磷酸二铵次之,磷酸三铵不稳定,不宜作肥料使用。
(1)用硫酸浸取磷灰石,利用了硫酸的__________等性质。
(2)操作 a 的名称是__________;装置a中要控制“N/P”,使反应能生成较多的一种酸式盐,其化学式为__________。
(3)固体 A 的化学式为__________,其用途有__________。
(4)操作b为__________、__________。
(5)磷铵属于________。 (填写“单一”或“复合”)
(6)操作C为过滤、洗涤、干燥,在洗涤过程中可选用下列试剂进行洗涤________ (选填字母),其优点是________。
(7)本工艺流程中操作 d 的目的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池由A、B、C、D四种金属按下表中装置图进行实验。
装置 |
|
|
|
现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是________________________________。
(2)装置乙中正极的电极反应式是________________________________。
(3)装置丙中溶液的pH________(填“变大”“变小”或“不变”)。
(4)四种金属活动性由强到弱的顺序是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)下图是实验室用氢气还原氧化铜实验的简易装置。其中的铜质燃烧匙可以在试管M中上下移动,实验时,先将细铜丝一端被弯成螺旋状,先在空气中加热变黑后再迅速伸入球型干燥管中。
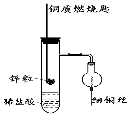

(1)铜质燃烧匙的作用有 , 。
(2)实验过程中,在试管M中可观察到的现象是 , 。
(二)原电池与电解池在化学工业中有广泛应用。如图装置,a为CuCl2溶液,X为Fe棒,Y为碳棒,回答以下问题:
(1)若断开k1,闭合k2,则装置为_____ ;X电极上的电极反应式为_____________;电解质溶液中的阳离子向______极移动(填X或Y);
(2)若线路中通过3.01×1022的电子,则Y极上析出物质的质量为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuCl是应用广泛的有机合成催化剂,工业上以制作印刷电路的废液(含Fe3+、Cu2+、Fe2+、Cl—)为原料生产CuCl的流程如下:
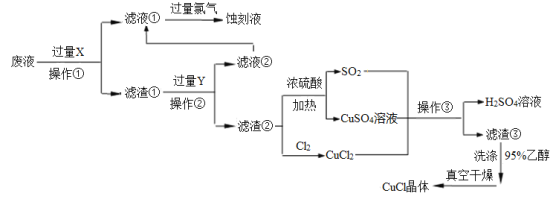
已知:CuCl是一种白色粉末,微溶于水,不溶于乙醇及稀硫酸,在水溶液中存在平衡:
CuCl(白色)+2Cl-![]() [CuCl3]2-(无色溶液);在空气中迅速被氧化成绿色;见光则分解,变成褐色。
[CuCl3]2-(无色溶液);在空气中迅速被氧化成绿色;见光则分解,变成褐色。
根据以上信息回答下列问题:
(1)试剂X是______,检验刻蚀液中金属阳离子的化学试剂是_____。(均填化学式)
(2)操作①、②、③相同,名称是________,所需要的主要玻璃仪器有烧杯、___ 、_____。
(3)滤渣①与Y反应的离子方程式为_________________。
(4)产生CuCl的化学方程式为_______________,当观察到 现象,即表明反应已经完全。
(5)在操作③之前往往向反应后的溶液中加入大量的水,其作用是 。
(6)在CuCl的生成过程中除环境问题、安全问题外,还应该注意的关键问题是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在t℃时,Ag2CrO4(橘红色)在水溶液中的沉淀溶解平衡曲线如下图所示。 又知AgCl的Ksp=1.8×10-10。下列说法正确的是( )
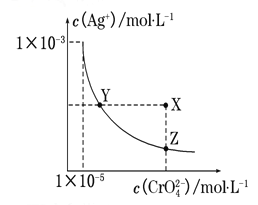
A.t℃时,Ag2CrO4的Ksp为1×10-8
B.在饱和Ag2CrO4溶液中加入K2CrO4能使溶液由Y点变为X点
C.t℃时,Y点和Z点时Ag2CrO4的Ksp相等
D.t℃时,将0.01 mol·L-1 AgNO3溶液滴入20 mL 0.01 mol·L-1 KCl和0.01 mol·L-1 K2CrO4的混合溶液中,CrO42-先沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
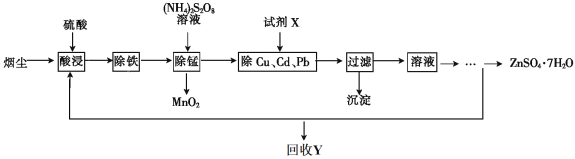
【题目】【化学——选修2化学与技术】将“废杂铜烟尘”用硫酸吸收浸取,既可保护环境又可得到用途广泛的高纯硫酸锌。已知烟尘中主要含ZnO,还有少量的FeO、Fe2O3、CuO、MnO、PbO、CdO。制备工艺流程如下:
已知:相关金属离子生成氢氧化物沉淀的pH及沉淀完全的pH如下表:
金属离子 | 开始沉淀的pH | 沉淀完全的pH |
Fe3+ | 1.1 | 3.2 |
Zn2+ | 5.5 | 8.0 |
Fe2+ | 5.8 | 8.8 |
(1)回收的产品Y是_____________________。
(2)“除铁”时,先加入_________________(氧化剂、还原剂),再将溶液的pH调整到__________。
(3)“除锰”时溶液中发生反应的化学方程式为____________________。
(4)除去Cu、Cd、Pb的同时可以回收一些重金属,试剂X为__________________。
(5)ZnSO4溶液经过__________、__________、过滤及干燥得到ZnSO4·7H2O。
(6)为了测定产品中ZnSO4·7H2O的含量,取ag产品溶于水,向所得溶液中慢慢加入碳酸钠溶液至沉淀完全;过滤、洗涤沉淀,在将沉淀固体煅烧至完全分解,称得为bg,则产品中ZnSO4·7H2O的质量分数是__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【实验化学】
己二酸( )是一种工业上具有重要意义的有机二元酸,在化工生产、有机合成工业、医药、润滑剂制造等方面都有重要作用,能够发生成盐反应、酯化反应等,并能与二元醇缩聚成高分子聚合物等,己二酸产量居所有二元羧酸中的第二位。实验室合成己二酸的反应原理和实验装置示意图如下:
)是一种工业上具有重要意义的有机二元酸,在化工生产、有机合成工业、医药、润滑剂制造等方面都有重要作用,能够发生成盐反应、酯化反应等,并能与二元醇缩聚成高分子聚合物等,己二酸产量居所有二元羧酸中的第二位。实验室合成己二酸的反应原理和实验装置示意图如下:
![]()

可能用到的有关数据如下:

实验步骤如下:
I、在三口烧瓶中加入16 mL 50%的硝酸(密度为1.31g/cm3),再加入1~2粒沸石,滴液漏斗中盛放有5.4 mL环己醇。
II、水浴加热三口烧瓶至50℃左右,移去水浴,缓慢滴加5~6滴环己醇,摇动三口烧瓶,观察到有红棕色气体放出时再慢慢滴加剩下的环己醇,维持反应温度在60℃~65℃之间。
III、当环己醇全部加入后,将混合物用80℃~90℃水浴加热约10min(注意控制温度),直至无红棕色气体生成为止。
IV、趁热将反应液倒入烧杯中,放入冰水浴中冷却,析出晶体后过滤、洗涤得粗产品。V、粗产品经提纯后称重为5.7g。
请回答下列问题:
(1)仪器a的名称为_ _。
(2)向三口烧瓶中滴加环己醇时,要控制好环己醇的滴入速率,防止反应过于剧烈导致温度迅速上升,否则可能造成较严重的后果,试列举一条可能产生的后果: _。
(3)已知用NaOH溶液吸收尾气时发生的相关反应方程式为:
2NO2+2NaOH=NaNO2+NaNO3+H2O NO+NO2+2NaOH =2NaNO2+H2O
如果改用纯碱溶液吸收尾气时也能发生类似反应,则相关反应方程式为(写一个即可):
________ ____。
(4)为了除去可能的杂质和减少产品损失,可分别用冰水和 洗涤晶体。
(5)粗产品可用 法提纯(填实验操作名称)。本实验所得到的己二酸产率为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
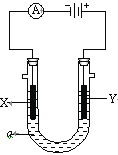
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
① 电解池中X极上的电极反应式为 。在X极附近观察到的现象是 。
② Y电极上的电极反应式为 ,检验该电极反应产物的方法是 。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,
① X电极的材料是 ,电极反应式是 。
② Y电极的材料是 ,电极反应式是 。(说明:杂质发生的电极反应不必写出)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com