
��ҵ�������е�һ����Ҫ��Ӧ��SO2��400-500���µĴ�����,2SO2(g)+O2(g) 2SO3(g),����һ������Ӧ���ȵĿ��淴Ӧ�������Ӧ���ܱ������н���,�����й�˵���д������
2SO3(g),����һ������Ӧ���ȵĿ��淴Ӧ�������Ӧ���ܱ������н���,�����й�˵���д������
| A���ﵽƽ��ʱ,SO2��Ũ����SO3��Ũ����� |
B����ͬ״���£���Ӧ2SO3(g)  2SO2(g)+O2(g)��һ�����ȷ�Ӧ 2SO2(g)+O2(g)��һ�����ȷ�Ӧ |
| C��Ϊ�����SO2ת����,���ʵ����O2Ũ�� |
| D�������¶ȣ����ȷ�Ӧ�������������ȷ�Ӧ������Ҳ���� |
 53���ò�ϵ�д�
53���ò�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��ͼ�ǿ��淴ӦX2 + 3Y2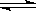 2Z2�ڷ�Ӧ�����еķ�Ӧ����V��ʱ�䣨t���Ĺ�ϵ���ߣ�����������ȷ����
2Z2�ڷ�Ӧ�����еķ�Ӧ����V��ʱ�䣨t���Ĺ�ϵ���ߣ�����������ȷ����
| A��t1ʱ��ֻ��������Ӧ |
| B��t2ʱ����Ӧ������ |
| C��t2- t3����Ӧ���ٷ��� |
| D��t2- t3�������ʵ�Ũ�Ȳ��ٷ����仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���淴Ӧ2NO2 2NO+O2�����������ܱ������з�Ӧ���ﵽƽ��״̬�ı�־��
2NO+O2�����������ܱ������з�Ӧ���ﵽƽ��״̬�ı�־��
�ٵ�λʱ��������n molO2��ͬʱ����2n mol NO2
����NO2��NO��O2�����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ���ʵı�Ϊ2��2��1��״̬
�ۻ���������ɫ���ٸı��״̬
�ܻ��������ܶȲ��ٸı��״̬
�ݻ�������ƽ����Է����������ٸı��״̬
| A���٢ۢ� | B���ڢۢ� | C���٢ۢ� | D���٢ڢۢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��C��CO2 2CO(����Ӧ����)������Ӧ�ķ�Ӧ����Ϊv1��N2��3H2
2CO(����Ӧ����)������Ӧ�ķ�Ӧ����Ϊv1��N2��3H2 2NH3(����Ӧ����)������Ӧ�ķ�Ӧ����Ϊv2������������Ӧ�����¶�����ʱ��v1��v2�ı仯���Ϊ
2NH3(����Ӧ����)������Ӧ�ķ�Ӧ����Ϊv2������������Ӧ�����¶�����ʱ��v1��v2�ı仯���Ϊ
| A��v1��С��v2���� | B��ͬʱ��С |
| C��v1����v2��С | D��ͬʱ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��֪�ֽ�1 mol H2O2 �ų�����98KJ���ں�����I������Һ�У�H2O2�ķֽ����Ϊ��
H2O2�� I�� ��H2O ��IO�� �� H2O2�� IO����H2O ��O2�� I�� ��
�����йط�Ӧ��˵����ȷ����( )
| A����Ӧ��������I����Ũ���й� | B��IO��Ҳ�Ǹ÷�Ӧ�Ĵ��� |
| C����Ӧ��ܵ���98KJ��mol��1 | D��v(H2O2)=v(H2O)=v(O2) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������,�� 4 mol A ����� 2 mol B ������ 2 L ���ܱ������л�ϲ���һ�������·������·�Ӧ��2A��g����B��g��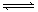 XC��g������ 2 s��Ӧ��ƽ��,��� C ��Ũ��Ϊ 0.6 mol��L��1 ��B�����ʵ���Ϊ1.4 mol,�������м���˵����
XC��g������ 2 s��Ӧ��ƽ��,��� C ��Ũ��Ϊ 0.6 mol��L��1 ��B�����ʵ���Ϊ1.4 mol,�������м���˵����
�������� A ��ʾ�ķ�Ӧ��ƽ������Ϊ 0.3 mol/(L��s)
�ڷ�Ӧǰ�����ڵ�ѹǿ��ƽ��������ڵ�ѹǿ֮��Ϊ1:1
�� 2 s ʱ����A��ת����Ϊ30�� �� X="2"
������ȷ����
| A���٢ۢ� | B���٢� | C���ڢ� | D���ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
ֻ�ı�һ��Ӱ�����أ�ƽ�ⳣ��K�뻯ѧƽ���ƶ��Ĺ�ϵ�����������
| A��Kֵ���䣬ƽ������ƶ� | B��Kֵ�仯��ƽ��һ���ƶ� |
| C��ƽ���ƶ���Kֵ���ܲ��� | D��ƽ���ƶ���Kֵһ���仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���ܱ������д�������ƽ�⣺CO(g)+H2O(g)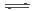 CO2(g)+H2(g)��CO2(g)��ƽ�����ʵ���Ũ��c(CO2)���¶�T�Ĺ�ϵ����ͼ��ʾ������˵���������
CO2(g)+H2(g)��CO2(g)��ƽ�����ʵ���Ũ��c(CO2)���¶�T�Ĺ�ϵ����ͼ��ʾ������˵���������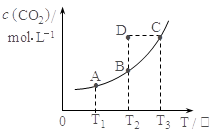
| A��ƽ��״̬A��C��ȣ�ƽ��״̬A��c(CO)С�� |
| B����T2ʱ������Ӧ����״̬D����һ����V����V�� |
C����ӦCO(g)+H2O(g)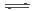 CO2(g)+H2(g) �Ħ�H��0 CO2(g)+H2(g) �Ħ�H��0 |
| D����T1��T2ʱ��ƽ�ⳣ���ֱ�ΪK1��K2����K1��K2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����˵����ȷ���ǣ� ��
| A������ѹǿ����ѧ��Ӧ����һ������ |
| B����ѧ��Ӧ����Ϊ��Ӧʱ���ڷ�Ӧ��Ũ�ȵ����ӻ���������Ũ�ȵļ��� |
| C�������¶ȣ���ѧ��Ӧ����һ������ |
| D�����뷴Ӧ���ѧ��Ӧ�������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com