
 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体).下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体).下列分析或结果错误的是( )| A. | 第二份溶液中最终溶质为FeSO4 | |
| B. | OA段产生的是NO,AB段的反应为Fe+2Fe3+═3Fe2+,BC段产生氢气 | |
| C. | 原混合酸中NO3- 物质的量为0.1 mol | |
| D. | H2SO4 浓度为2.5 mol•L-1 |
分析 由图象可知,由于铁过量,OA段发生反应为:Fe+NO3-+4H+=Fe3++NO↑+2H2O,AB段发生反应为:Fe+2Fe3+=3Fe2+,BC段发生反应为:Fe+2H+=Fe2++H2↑.
A.铁先与硝酸反应,之后铁与铁离子反应生产亚铁离子,最后是铁和硫酸反应,铁单质全部转化为亚铁离子,硝酸全部起氧化剂作用,没有显酸性的硝酸;
B.铁先与硝酸反应生成一氧化氮与铁离子,之后铁与铁离子反应生产亚铁离子,最后是铁和硫酸反应;
C.OA段发生反应为:Fe+NO3-+4H+=Fe3++NO↑+2H2O,硝酸全部起氧化剂作用,根据铁的物质的量结合离子方程式计算;
D.根据铁和硫酸的反应中铁的质量来确定所需硫酸的量,进而确定硫酸的浓度.
解答 解:由图象可知,由于铁过量,OA段发生反应为:Fe+NO3-+4H+=Fe3++NO↑+2H2O,AB段发生反应为:Fe+2Fe3+=3Fe2+,BC段发生反应为:Fe+2H+=Fe2++H2↑.
A.硝酸全部被还原,没有显酸性的硝酸,因为溶液中有硫酸根,并且铁单质全部转化为亚铁离子,所以溶液中最终溶质为FeSO4,故A正确;
B.由图象可知,由于铁过量,OA段发生反应为:Fe+NO3-+4H+=Fe3++NO↑+2H2O,AB段发生反应为:Fe+2Fe3+=3Fe2+,BC段发生反应为:Fe+2H+=Fe2++H2↑,故B正确;
C.OA段发生反应为:Fe+NO3-+4H+=Fe3++NO↑+2H2O,硝酸全部起氧化剂作用,所以n(NO3-)=2n(Fe)=2×$\frac{11.2g}{56g/mol}$=0.4mol,故C错误;
D.反应消耗14g铁,也就是$\frac{14g}{56g/mol}$=0.25mol,所有的铁都在硫酸亚铁中,根据硫酸根守恒,所以每份含硫酸0.25mol,所以硫酸的浓度是$\frac{0.25mol}{0.1L}$=2.5mol/L,故D正确.
故选C.
点评 本题以图象为载体,考查有关金属和酸反应的计算题,难度较大,关键根据图象分析各段发生的反应,注意与铁的反应中硝酸全部起氧化剂作用,


 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 人造纤维、合成纤维和光导纤维都是有机高分子化合物 | |
| B. | 煤经过气化、液化等物理变化可得到清洁燃料 | |
| C. | 煤的干馏、石油裂化、石油裂解都是化学变化 | |
| D. | 棉花、羊毛、蚕丝、麻都由C、H、O元素构成 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
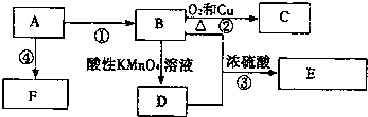
 ,F的结构简式
,F的结构简式 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某同学想研究氨基酸的分离和鉴定的方法,已知实验室中有0.5%的赖氨酸、脯氨酸、缬氨酸、苯丙氨酸、亮氨酸溶液以及它们的混合液(各组份浓度均为0.5% );现提供如下器材和试剂:
某同学想研究氨基酸的分离和鉴定的方法,已知实验室中有0.5%的赖氨酸、脯氨酸、缬氨酸、苯丙氨酸、亮氨酸溶液以及它们的混合液(各组份浓度均为0.5% );现提供如下器材和试剂:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 (1)写出葡萄糖发生银镜反应的化学方程式CH2OH(CHOH)4CHO+2Ag(NH3)2OH $\stackrel{加热}{→}$CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O.
(1)写出葡萄糖发生银镜反应的化学方程式CH2OH(CHOH)4CHO+2Ag(NH3)2OH $\stackrel{加热}{→}$CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓H2SO4滴在白纸上发黑,说明弄浓H2SO4具有脱水性 | |
| B. | 浓H2SO4和浓HCl混合可制氯化氢,说明浓H2SO4具有吸水性 | |
| C. | 常温下,浓H2SO4可以用铝罐贮存,说明铝与浓H2SO4不反应 | |
| D. | 反应CuSO4+H2S→CuS+H2SO4能在溶液中完全进行,证明CuS既不溶于水也不溶于稀H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L pH=1的乙酸溶液中H+数小于0.1NA | |
| B. | 标准状况下,22.4L乙醇的分子数为NA | |
| C. | 28g乙烯和丙烯所含碳氢键的数目为4NA | |
| D. | 1 mol 甲基所含的电子数为10NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com